第二课时离子反应学习目标:1
通过BaCl2溶液与Na2SO4溶液的反应现象,认识离子反应的本质
通过实验事实认识离子反应发生的条件
会书写离子方程式并能进行正误判断
理解离子方程式的意义
掌握一些常见离子能否共存的判断方法
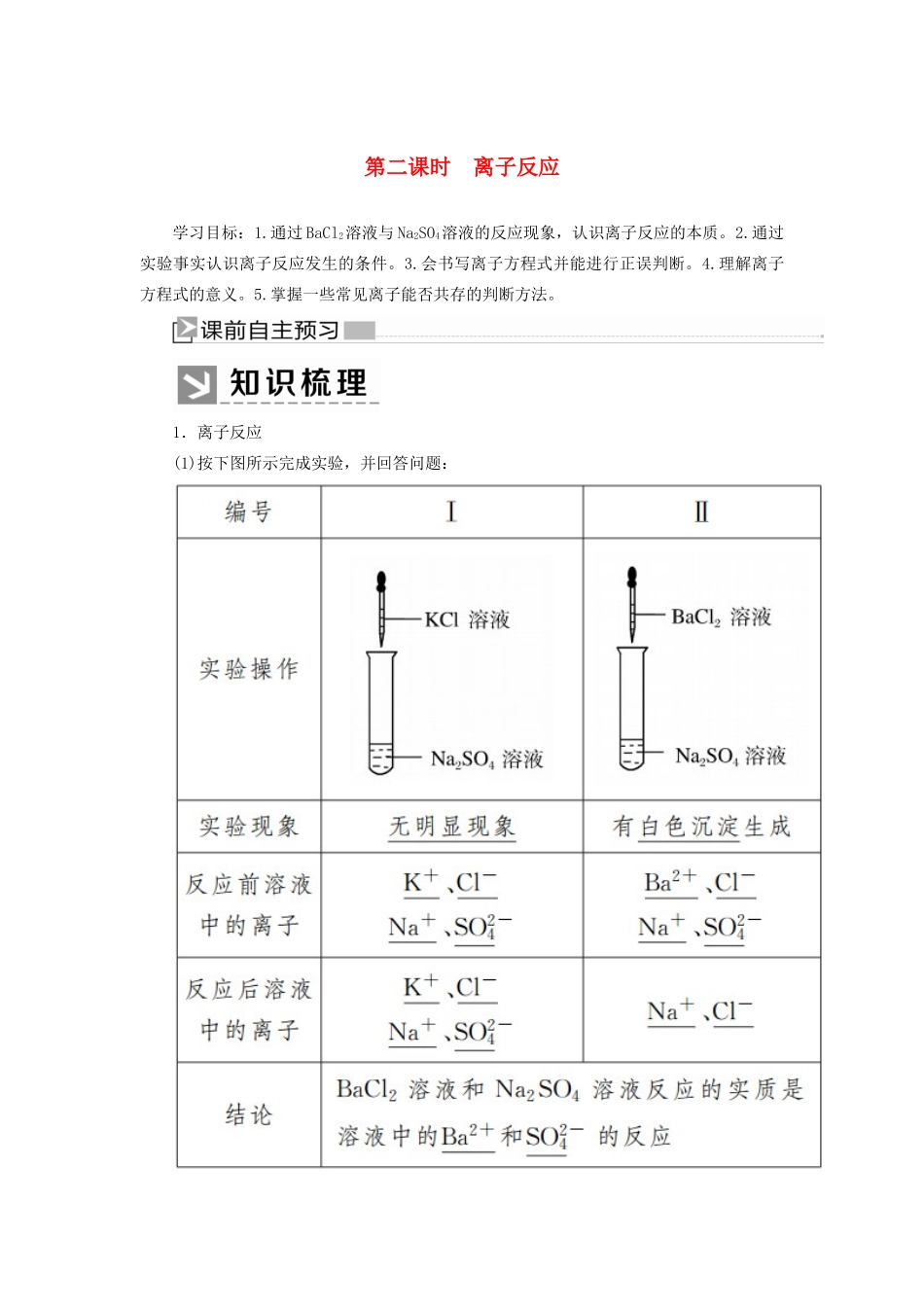
1.离子反应(1)按下图所示完成实验,并回答问题:(2)概念:电解质在溶液中的反应实质上是离子之间的反应,这种反应属于离子反应
2.离子方程式(1)概念:用实际参加反应的离子符号来表示反应的式子
(2)书写步骤:以Na2SO4溶液和BaCl2溶液反应为例
①写:正确书写反应的化学方程式:Na2SO4+BaCl2===BaSO4↓+2NaCl
②拆:把易溶于水且易电离的物质拆写成离子的形式:2Na++SO+Ba2++2Cl-===BaSO4↓+2Na++2Cl-
③删:删去方程式两边不参加反应的离子,并将化学计量数化为最简整数比:Ba2++SO===BaSO4↓
④查:检查方程式两边各元素的原子个数和电荷总数是否相等
(3)意义①写出表中几种不同的酸与不同的碱发生反应的离子方程式
化学方程式离子方程式NaOH+HCl===NaCl+H2OH++OH-===H2OKOH+HCl===KCl+H2OH++OH-===H2O2NaOH+H2SO4===Na2SO4+2H2OH++OH-===H2O2KOH+H2SO4===K2SO4+2H2OH++OH-===H2O②结论离子反应方程式不仅可以表示某个具体的化学反应,还可以表示同一类型的离子反应
1.判断正误(正确的打“√”,错误的打“×”)(1)硫酸铜溶液与氯化钡溶液反应的实质是SO与Ba2+生成了BaSO4沉淀()(2)碳酸钙与盐酸反应的离子方程式为CO+2H+===H2O+CO2↑()(3)浓盐酸与铁屑反应的离子方程式为2Fe+3H+===2Fe3++3H2↑()(4)Ag++Cl-===