铁及其化合物明考纲1.以“氧化还原反应”为主线掌握“铁三角”及其应用
2.掌握过渡元素的单质及化合物的基本特点
3.掌握变价金属元素离子的氧化性和还原性及检验方法
4.掌握Fe(OH)2的制备
析考情铁元素是过渡元素的代表,而铁及铁合金材料又在工农业生产中有着重要应用,因此铁及其化合物的有关知识是高考的热点内容之一,预计命题以生活、生产、实际应用为背景,突出铁及其化合物的性质、应用为主,题型延续选择题、填空题、综合推断题及实验探究题的形式
考点用物质分类思想认识铁及其重要化合物一、铁的单质1.铁的位置、结构、化合价(1)周期表中的位置:第四周期第Ⅷ族;原子结构示意图:
(2)在参加化学反应时,铁易失去最外层上的2个电子,有时它还失去次外层上的一个电子,所以铁有+2、+3两种价态,且+3价稳定
2.铁的物理性质和存在纯净的铁是银白色的金属,铁的熔点较高
当含有碳和其它元素时,熔点将降低,导电性比铜、铝差
铁能被磁铁吸引,在磁场作用下,铁自身也能产生磁性
铁在地壳中的含量占第4位
自然界中铁元素主要以化合态形式存在
重要的铁矿石有(填化学式):赤铁矿Fe2O3,磁铁矿Fe3O4,褐铁矿2Fe2O3·3H2O,菱铁矿FeCO3
3.铁的化学性质铁单质性质活泼,有较强的还原性,铁元素主要化合价为+2价和+3价
(1)与非金属单质的反应①与O2的反应常温:铁被腐蚀生成铁锈,其主要成分为Fe2O3
点燃:3Fe+2O2=====Fe3O4,现象:剧烈燃烧,火星四射,生成黑色固体
②与Cl2的反应:2Fe+3Cl2=====2FeCl3,现象:生成棕黄色的烟
③与S的反应:Fe+S=====FeS,现象:生成黑色固体
(2)与水的反应常温下铁与水不反应,在高温条件下与水蒸气反应:3Fe+2H2O(g)=====Fe3O4+4H2
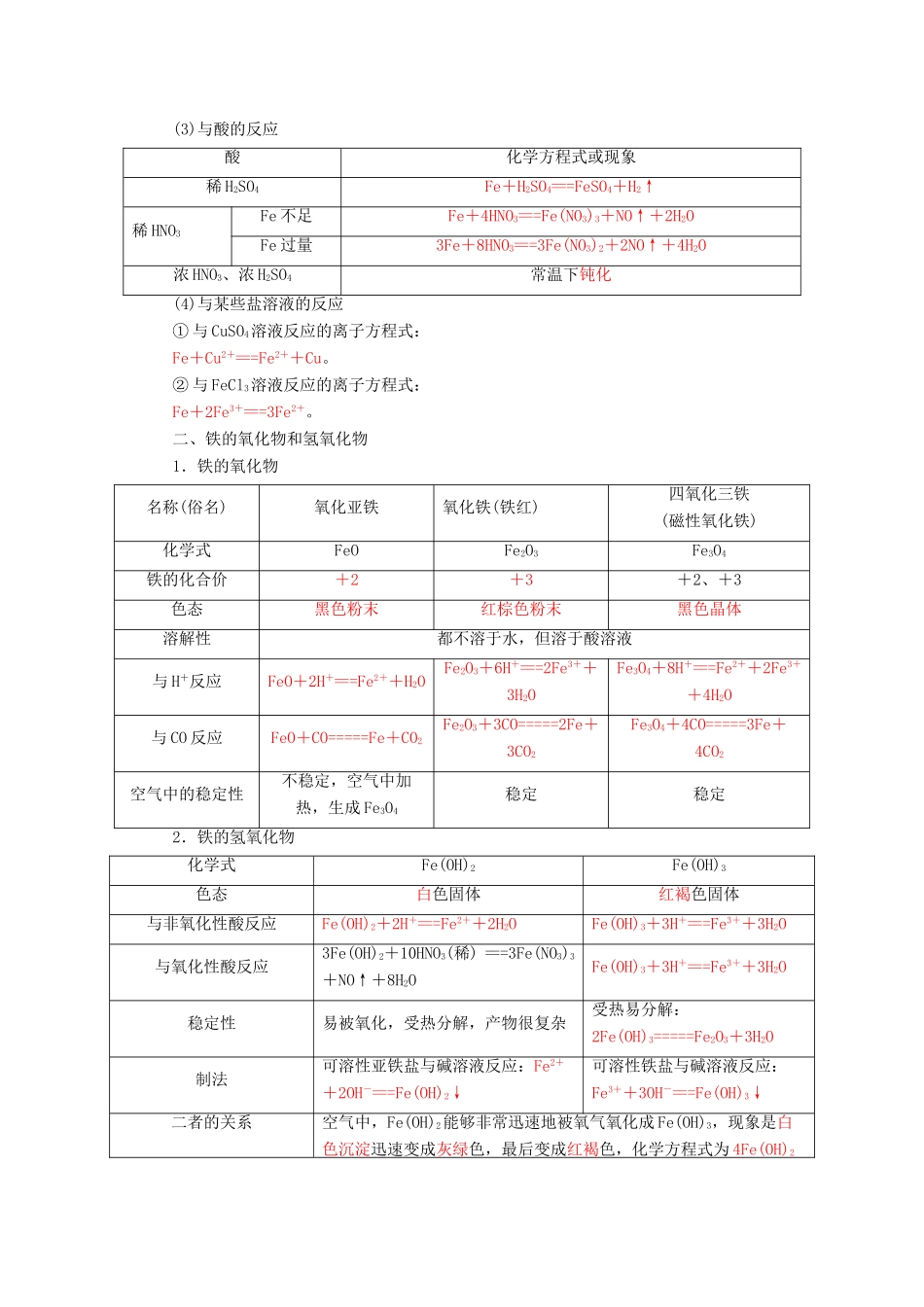
(3)与酸的反应酸化学方程式或现象稀H2SO4Fe+H2S