第1节碳的多样性考纲定位全国卷5年考情1
掌握碳单质及其重要化合物的主要性质及应用
了解碳单质及其重要化合物对环境质量的影响
了解碳及其重要化合物的制备方法
2017年:Ⅱ卷T13(B);Ⅲ卷T11(C)2016年:Ⅰ卷T8(D);Ⅱ卷T7、T12;Ⅲ卷T7(A)2015年:Ⅰ卷T26;Ⅱ卷T10(B)、T13(D)2014年:Ⅰ卷T8、T13(CD);Ⅱ卷T7(A、B)、T9(B)、T10(B、C)2013年:Ⅰ卷T7(D);Ⅱ卷T9(B)、T10(C)考点1|碳单质及其氧化物的性质(对应学生用书第47页)[考纲知识整合]1.碳元素的原子结构与存在碳元素位于元素周期表中第2周期ⅣA族,原子结构示意图为在自然界中既有游离态的碳又有化合态的碳
2.碳单质的多样性(1)同素异形体由同一种元素组成的性质不同的单质
碳元素的同素异形体有C60、石墨、金刚石,氧元素的有O2和O3,磷元素的有红磷和白磷
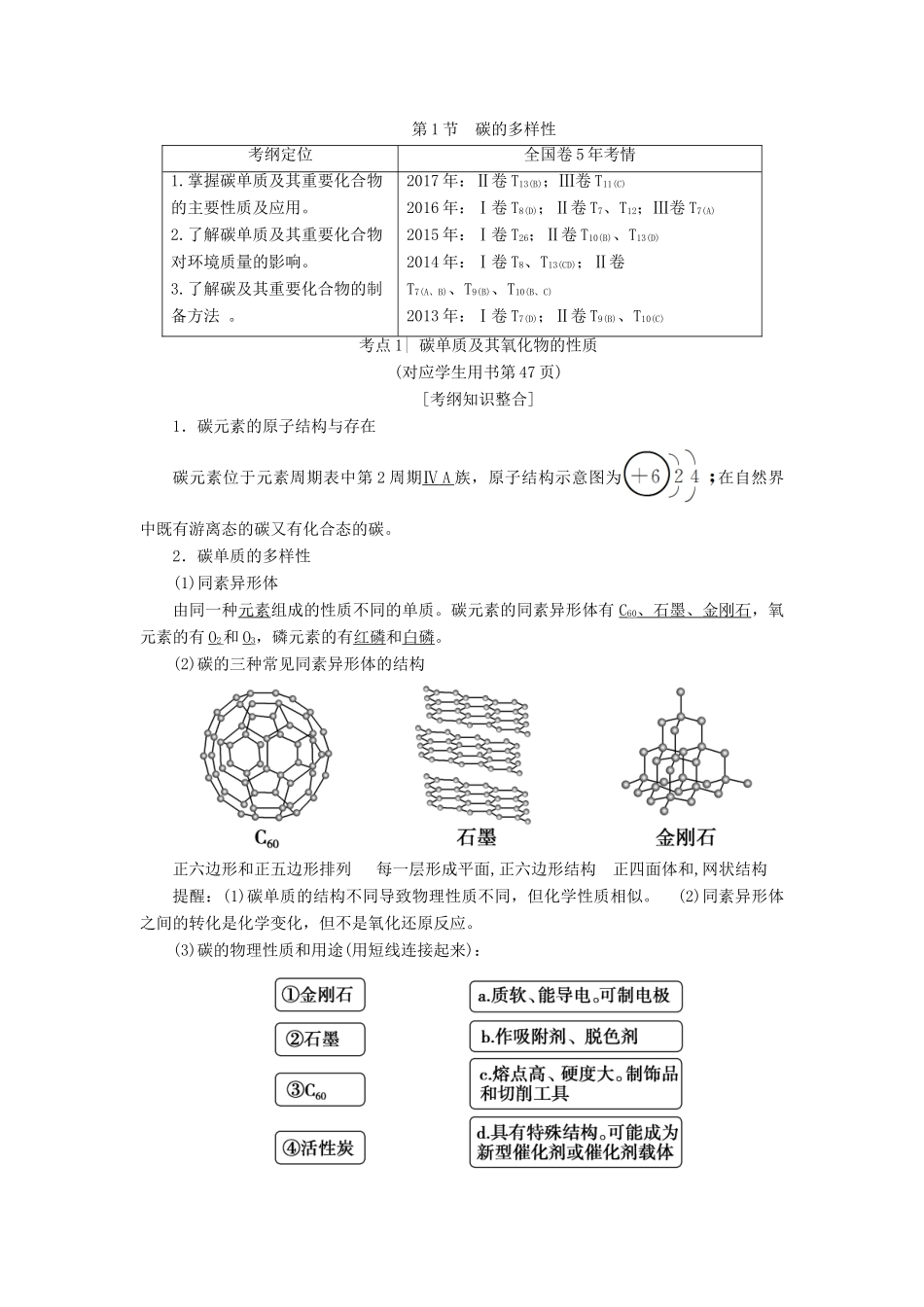
(2)碳的三种常见同素异形体的结构正六边形和正五边形排列每一层形成平面,正六边形结构正四面体和,网状结构提醒:(1)碳单质的结构不同导致物理性质不同,但化学性质相似
(2)同素异形体之间的转化是化学变化,但不是氧化还原反应
(3)碳的物理性质和用途(用短线连接起来):【提示】①—c②—a③—d④—b(4)碳单质的化学性质:①与O2的反应(用化学方程式表示):O2不足:2C+O2=====2CO
O2充足:C+O2=====CO2
②与其他物质的反应(用化学方程式表示):与CuO反应:2CuO+C=====2Cu+CO2↑(可用于金属的冶炼);与SiO2反应:SiO2+2C=====Si+2CO↑
与CO2反应:C+CO2=====2CO(用于炼铁还原剂的制备);与水蒸气反应:C+H2O(g)=====CO+H2(制水煤气)
与浓硫酸反应:C+2H2SO4(浓)=====CO2↑