第三章烃的含氧衍生物第三节羧酸酯第1课时羧酸●新知导学1.羧酸的定义及分类(1)定义:由烃基和羧基相连构成的有机化合物
(2)通式:R-COOH,官能团-COOH
饱和一元羧酸的通式:CnH2n+1COOH或CnH2nO2(3)分类①按分子中烃基的结构分类CH3COOHC17H35COOHC17H33COOH②按分子中羧基的数目分类HCOOHHOOC-COOH(4)通性羧酸分子中都含有羧基官能团,因此都具有酸性,都能发生酯化反应
2.乙酸(1)俗名:醋酸;分子式:C2H4O2;结构简式:CH3COOH或
(2)物理性质颜色状态气味溶解性熔点无色液体有刺激性气味易溶于水和乙醇16
6℃,温度低时凝结成冰样晶体,又称冰醋酸(3)化学性质①酸性:电离方程式为CH3COOHCH3COO-+H+A.与酸碱指示剂反应:乙酸能使紫色石蕊试液变红B.与活泼金属反应:Zn+2CH3COOH―→(CH3COO)2Zn+H2↑C.与碱反应:CH3COOH+NaOH―→CH3COONa+H2OD.与碱性氧化物反应:CuO+2CH3COOH―→(CH3COO)2Cu+H2OE.与某些盐反应:CaCO3+2CH3COOH―→(CH3COO)2Ca+H2O+CO2↑②酯化反应(或取代反应)
A.含义:酸和醇作用生成酯和水的反应
B.断键方式:酸脱氢,醇脱羟基
C.乙酸与乙醇的反应:CH3COOH+CH3CH2OHCH3COOC2H5+H2O
●自主探究1.甲酸中含有什么官能团
据此推测甲酸有哪些性质
提示:对甲酸的分子结构进行分析:可知,甲酸中含有羟基、羧基和醛基,因此甲酸除有一般羧酸的性质外,还有醛的还原性
2.等碳原子的饱和一元羧酸与饱和一元酯的分子通式是什么
两类物质属于什么关系
提示:均为CnH2nO2,互为同分异构体,如CH3COOH与HCOOCH3
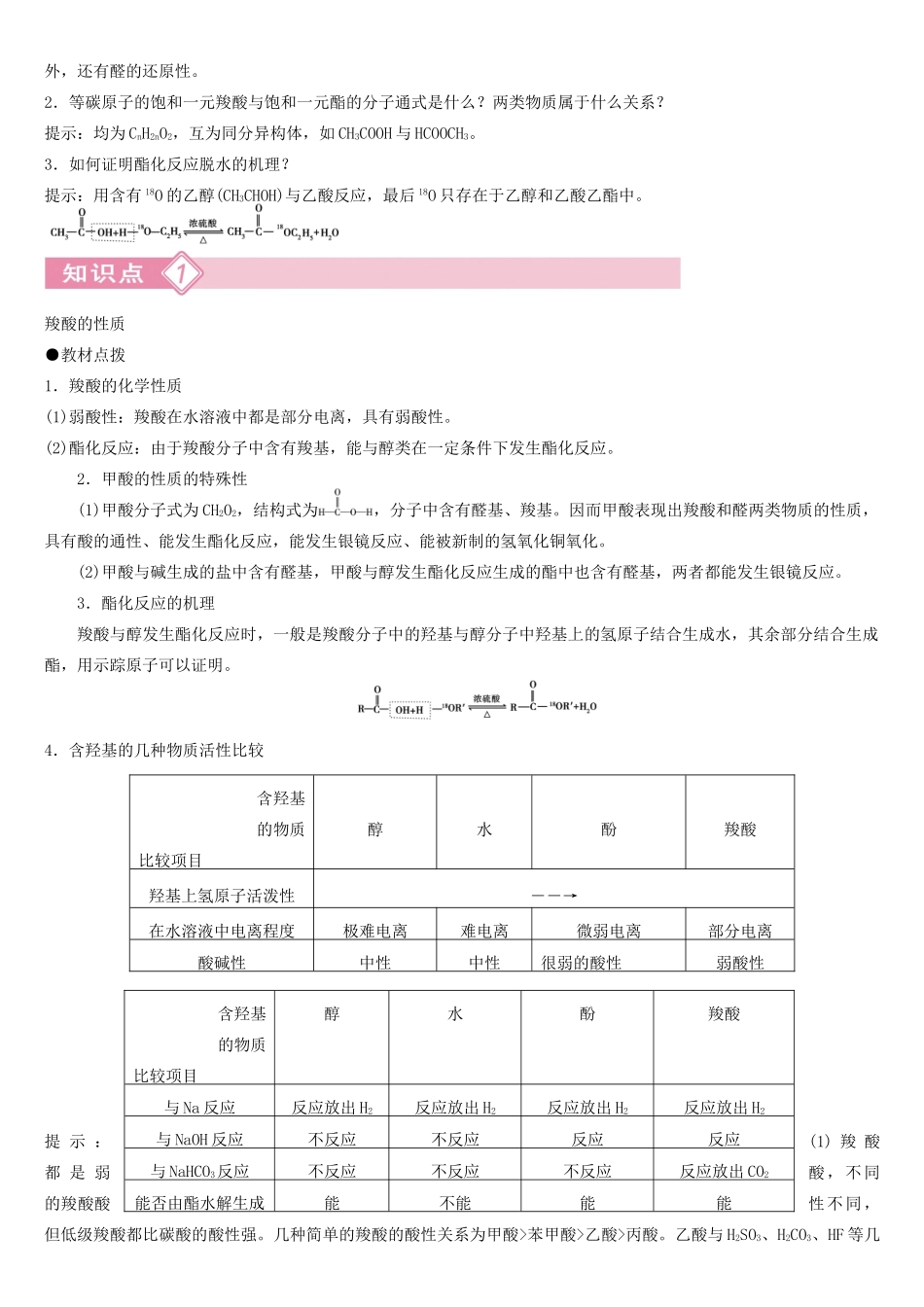
3.如何证明酯化反应脱水的机理