第三节硫及其重要化合物最新考纲:1
掌握硫元素的单质及其重要化合物的主要性质及应用
了解硫元素的单质及其重要化合物的制备方法
了解二氧化硫对环境质量的影响
核心素养:1
宏观辨识与微观探析:能从不同层次认识硫单质及化合物的多样性,并对其进行分类
科学探究与创新意识:能根据硫单质及化合物的性质提出有探究价值的问题;从问题和假设出发,确定探究目的,设计探究方案,进行实验探究
知识点一硫及其氧化物性质1.自然界中硫元素的存在2.硫的物理性质3
硫的化学性质H2S――→――→SO2(3)与强氧化剂反应(如浓硫酸):S+2H2SO4(浓)=====3SO2↑+2H2O,表现还原性
(4)与碱溶液反应:3S+6NaOH=====2Na2S+Na2SO3+3H2O,表现氧化性和还原性
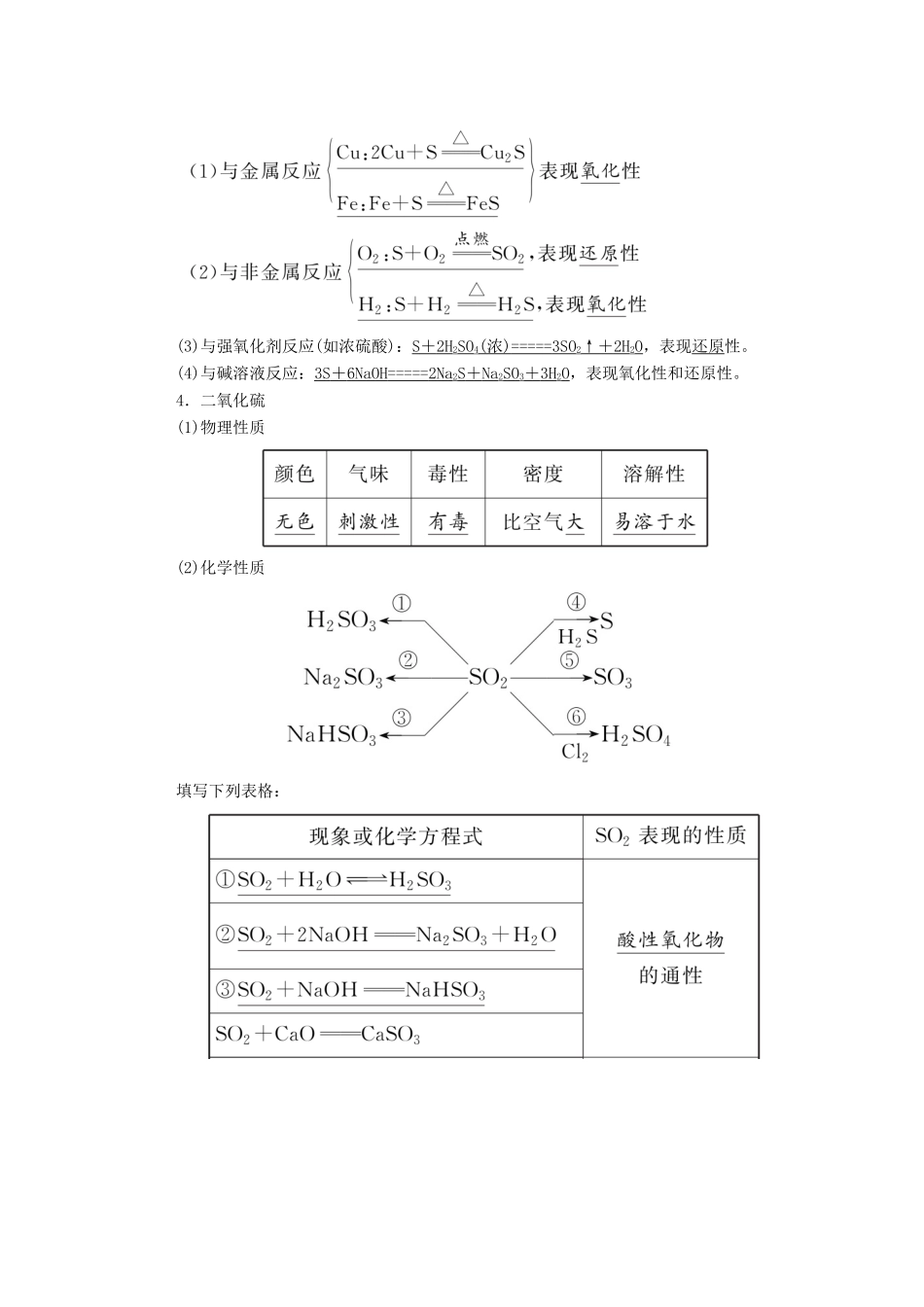
4.二氧化硫(1)物理性质(2)化学性质填写下列表格:(3)SO2对大气的污染与防治①酸雨的形成过程:②SO2对大气的污染与防治:5.三氧化硫(1)物理性质:熔点16
8℃,沸点44
8℃,在常温下为液态,在标准状况下为固态
(2)化学性质判断正误(正确的打“√”,错误的打“×”)1.Na、O、S三种元素形成的一种盐溶于水后加入稀盐酸,有黄色沉淀析出,同时产生有刺激性气味的气体(√)2.下列物质的转化在一定条件下能够实现:S――→SO3――→H2SO4(×)提示:S燃烧只能生成SO2
3.SO2和SO3混合气体通入Ba(NO3)2溶液可得到BaSO3和BaSO4(×)4.硫和氯气分别与铁反应后铁元素的价态相同(×)提示:S与Fe反应生成FeS,Cl2与Fe反应生成FeCl3
5.SO2通入品红溶液中褪色的原理与SO2通入溴水中褪色的原理相同(×)提示:SO2通入品红溶液中体现漂白性,SO2通入溴水中体现其还原性
6.洗涤附着在试管内壁上的硫用CS2或热的浓NaOH溶液(√)7.除去CO2中的SO