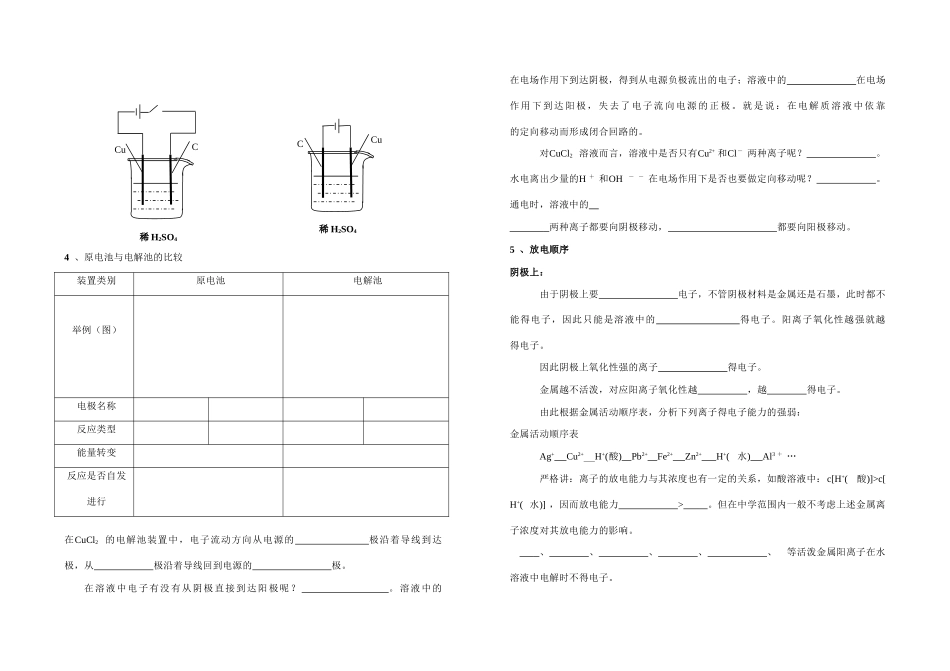
CCCH3CH2OH稀H2SO4FeC稀H2SO4玻璃棒玻璃棒第三节电解池一、电解原理1、试验探究如图所示:与电源正极相连的电极叫极,与电源负极相连的电极叫极
若烧杯中的液体为CuCl2溶液,合上电源开关,能否看到小灯泡发光
给CuCl2溶液通电时现象:阴极上,经检验该物质是
阳极上:,经检验该物质是
两支电极上发生的反应为:阳极:
反应类型:反应
反应类型:反应
过程分析:CuCl2溶液能导电是因为存在,通电后这些自由移动的离子,在电场作用下作移动,根据相互吸引的原理,带负电的氯离子向极移动,在阳极,氯离子失去电子被为氯原子,并两两结合成氯分子,从阳极放出,带正电的铜离子向极移动,在阴极铜离子获得电子被成铜原子,覆盖在阴极上
2、电解:使电流通过溶液而在阴、阳两极引起的过程
所用电流一般为直流电还是交流电较好
该过程中能转化为能
这是一个物理过程还是一个化学过程
显然:电解质溶液的导电过程就是的过程
3、电解池:将能转化为能的装置
构成电解池的条件:①②③④判断下列装置是否属于电解池:CuCl2溶液CC×稀H2SO4CuC稀H2SO4CCu4、原电池与电解池的比较装置类别原电池电解池举例(图)电极名称反应类型能量转变反应是否自发进行在CuCl2的电解池装置中,电子流动方向从电源的极沿着导线到达极,从极沿着导线回到电源的极
在溶液中电子有没有从阴极直接到达阳极呢
溶液中的在电场作用下到达阴极,得到从电源负极流出的电子;溶液中的在电场作用下到达阳极,失去了电子流向电源的正极
就是说:在电解质溶液中依靠的定向移动而形成闭合回路的
对CuCl2溶液而言,溶液中是否只有Cu2+和Cl-两种离子呢
水电离出少量的H+和OH--在电场作用下是否也要做定向移动呢
通电时,溶液中的两种离子都要向阴极移动,都要向阳极移动
5、放电顺序阴极上:由于阴极上要电