第2课时沉淀反应的应用[目标导航]1
能用平衡移动原理分析理解沉淀的溶解与生成、沉淀转化的实质
学会用沉淀溶解平衡的移动解决生产、生活中的实际问题
1.沉淀的生成(1)调节pH法如加入氨水调节pH=4,可除去氯化铵中的杂质氯化铁
反应离子方程式:Fe3++3NH3·H2O===Fe(OH)3↓+3NH
(2)加沉淀剂法以Na2S、H2S等作沉淀剂,使Cu2+、Hg2+等生成极难溶的硫化物CuS、HgS等沉淀
反应离子方程式如下:①加Na2S生成CuS:S2-+Cu2+===CuS↓
②通入H2S生成CuS:H2S+Cu2+===CuS↓+2H+
2.沉淀的溶解(1)原理:根据平衡移动原理,对于在水中难溶的电解质,只要不断移去溶解平衡体系中的相应离子,平衡就向沉淀溶解的方向移动,从而使沉淀溶解
(2)实例:①CaCO3沉淀溶于盐酸中:CO2气体的生成和逸出,使CaCO3溶解平衡体系中的CO浓度不断减小,平衡向沉淀溶解的方向移动
②分别写出用HCl溶解难溶电解质FeS、Al(OH)3、Cu(OH)2的离子方程式FeS+2H+===Fe2++H2S↑、Al(OH)3+3H+===Al3++3H2O、Cu(OH)2+2H+===Cu2++2H2O
③向Mg(OH)2悬浊液中分别滴加蒸馏水、稀盐酸、NH4Cl溶液,白色沉淀将不溶解、溶解、溶解(填“溶解”或“不溶解”)
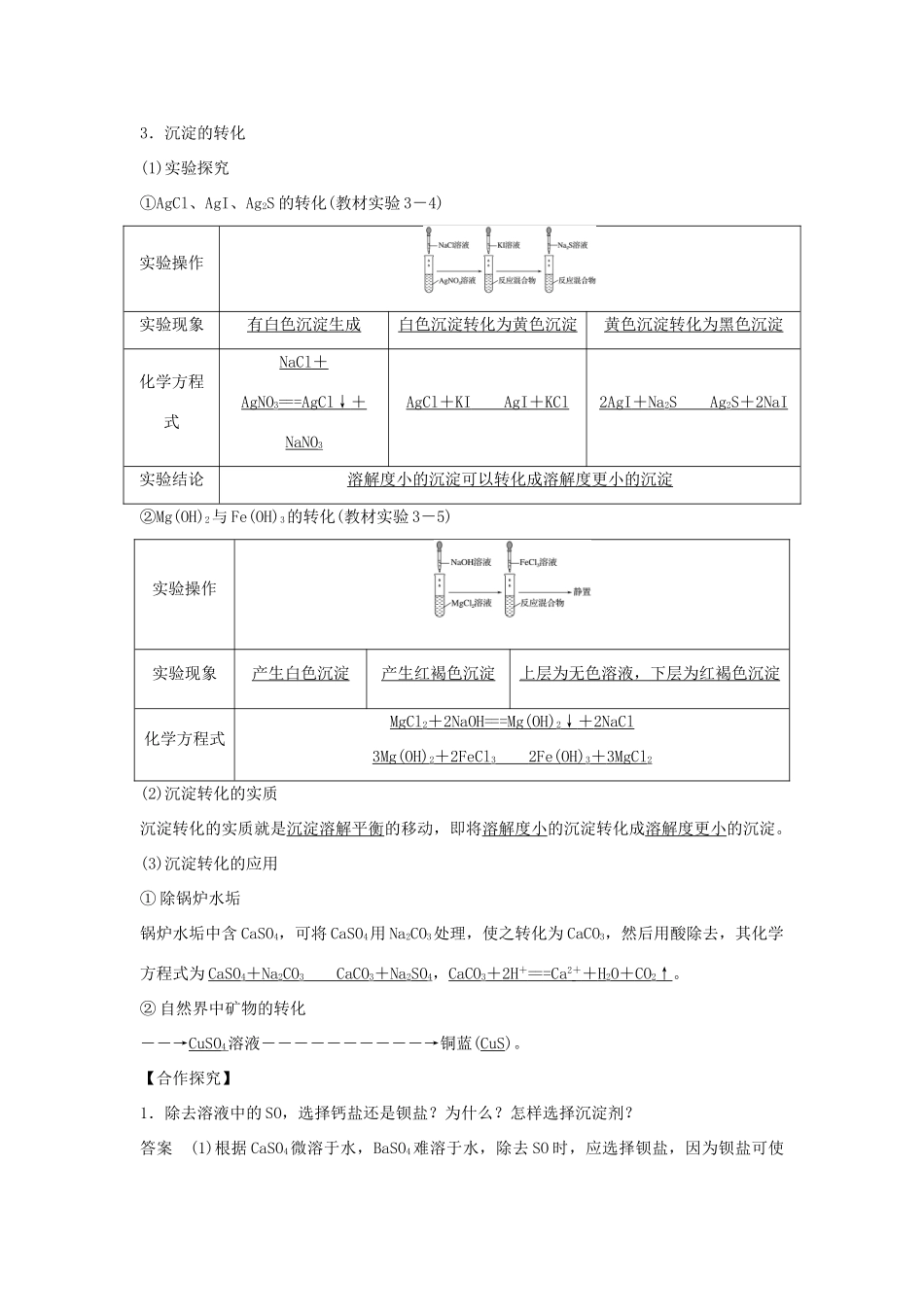
3.沉淀的转化(1)实验探究①AgCl、AgI、Ag2S的转化(教材实验3-4)实验操作实验现象有白色沉淀生成白色沉淀转化为黄色沉淀黄色沉淀转化为黑色沉淀化学方程式NaCl+AgNO3===AgCl↓+NaNO3AgCl+KIAgI+KCl2AgI+Na2SAg2S+2NaI实验结论溶解度小的沉淀可以转化成溶解度更小的沉淀②Mg(OH)2与Fe(OH)3的转化(教材实验3-5)实验操作实验现象产生白色沉淀产