(八)氨气的实验室制法及性质探究(对应学生用书第57页)突破1|氨气的实验室制法[考纲知识整合]1.NH3的一般实验室制法(1)原理:2NH4Cl+Ca(OH)2=====CaCl2+2NH3↑+2H2O
注:①不能用NH4NO3,因NH4NO3受热爆炸;②Ca(OH)2不能用KOH或NaOH代替,因两者易吸湿,易结块,不利于产生NH3,且高温下腐蚀试管
③不能只用NH4Cl固体加热制取NH3,因为NH4Cl受热分解生成的NH3和HCl遇冷又化合成NH4Cl
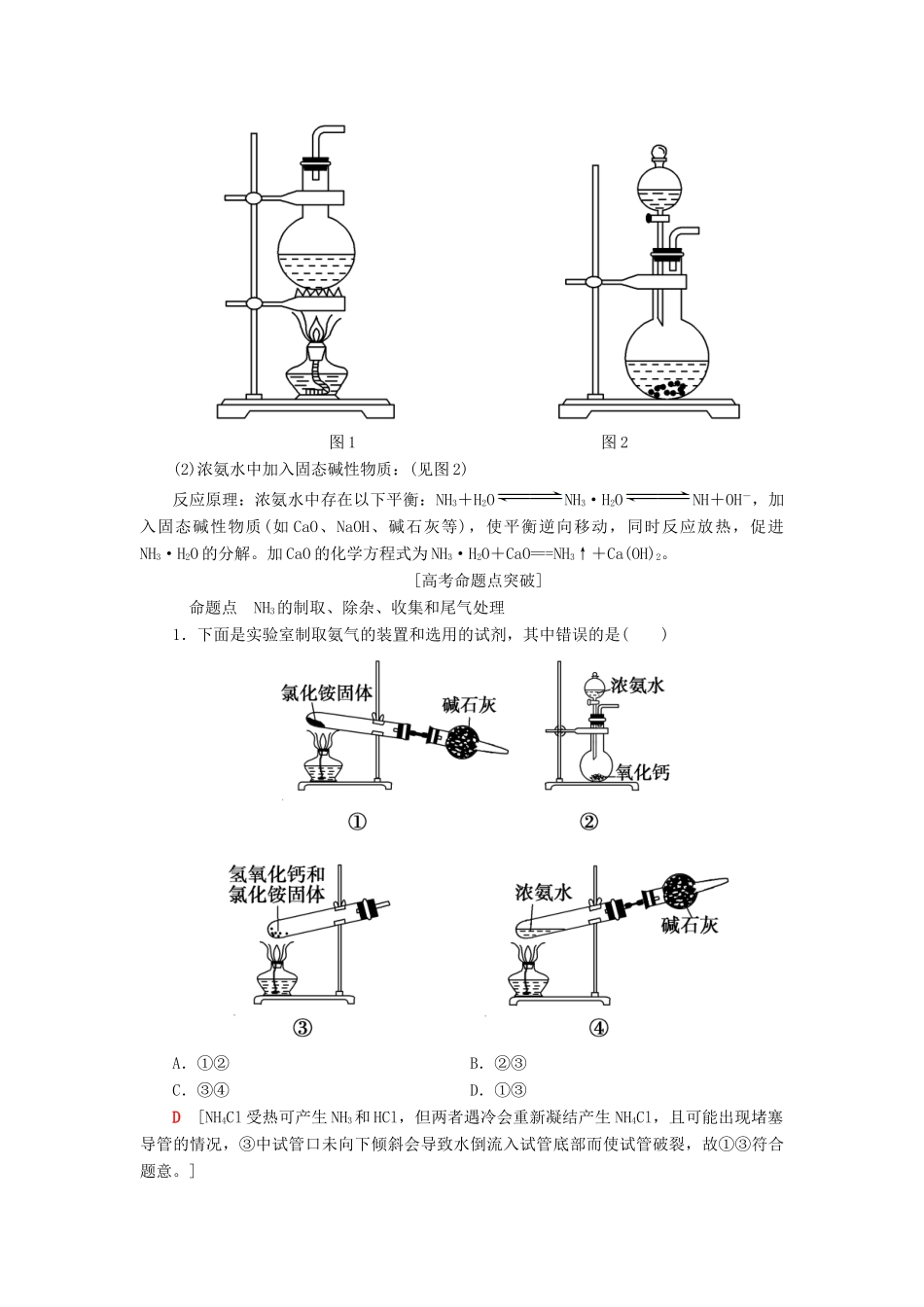
(2)实验装置2.两种简易方法(1)加热浓氨水:(见图1)反应原理:NH3·H2O=====NH3↑+H2O
图1图2(2)浓氨水中加入固态碱性物质:(见图2)反应原理:浓氨水中存在以下平衡:NH3+H2ONH3·H2ONH+OH-,加入固态碱性物质(如CaO、NaOH、碱石灰等),使平衡逆向移动,同时反应放热,促进NH3·H2O的分解
加CaO的化学方程式为NH3·H2O+CaO===NH3↑+Ca(OH)2
[高考命题点突破]命题点NH3的制取、除杂、收集和尾气处理1.下面是实验室制取氨气的装置和选用的试剂,其中错误的是()A.①②B.②③C.③④D.①③D[NH4Cl受热可产生NH3和HCl,但两者遇冷会重新凝结产生NH4Cl,且可能出现堵塞导管的情况,③中试管口未向下倾斜会导致水倒流入试管底部而使试管破裂,故①③符合题意
]2.下列装置用于实验室中制取干燥氨气的实验,能达到实验目的的是()【导学号:95160057】A.用装置甲收集,检验氨气B.用装置乙除去氨气中少量水蒸气C.用装置丙收集氨气D.用装置丁吸收多余的氨气D[检验氨气用湿润红色石蕊试纸变蓝,A项错误;氨气和浓硫酸反应生成硫酸铵,不能用浓硫酸干燥氨气,B项错误;收集氨气的烧瓶不应密闭,C项错误;氨气极易溶于水,用水吸收氨气时要注意防倒吸,可用丁装置