第1课时浓度、压强对化学反应速率的影响学习目标1
知道活化能的含义及其对化学反应速率的影响
了解浓度、压强等条件对化学反应速率的影响
学习过程【自主学习1】结合生活实践与已经掌握的知识,请同学归纳有哪些因素对化学速率产生影响
影响化学反应速率的内因有
影响化学反应速率的外因主要有
探究一:浓度对反应速率的影响【实验探究】做以下两个实验并结合教材第20页,实验2—2讨论总结
取两支试管,分别加入少量大理石,再分别加入10mL1mol·L-1的盐酸和10mL0
1mol·L-1的盐酸
取两支试管分别加入少量铁片,再分别加入10mL1mol·L-1的盐酸和10mL0
1mol·L-1的盐酸
【小结】实验证明,在其他条件相同时,增大反应物浓度,反应速率会;减小反应物浓度,反应速率会
【复习回顾】有效碰撞模型在其他条件不变时,对于某一反应来说,活化分子在反应物分子中所占的百分数(即)是一定的
化学反应速率与分子间的有关,因此所有能够改变、以及的外界条件,都可以用来、反应的速率
、、、使用等是我们已经用过的方法
【总结】当反应物浓度时,单位体积内反应物分子,单位体积内活化分子数目也相应,单位时间内有效碰撞次数,化学反应速率就
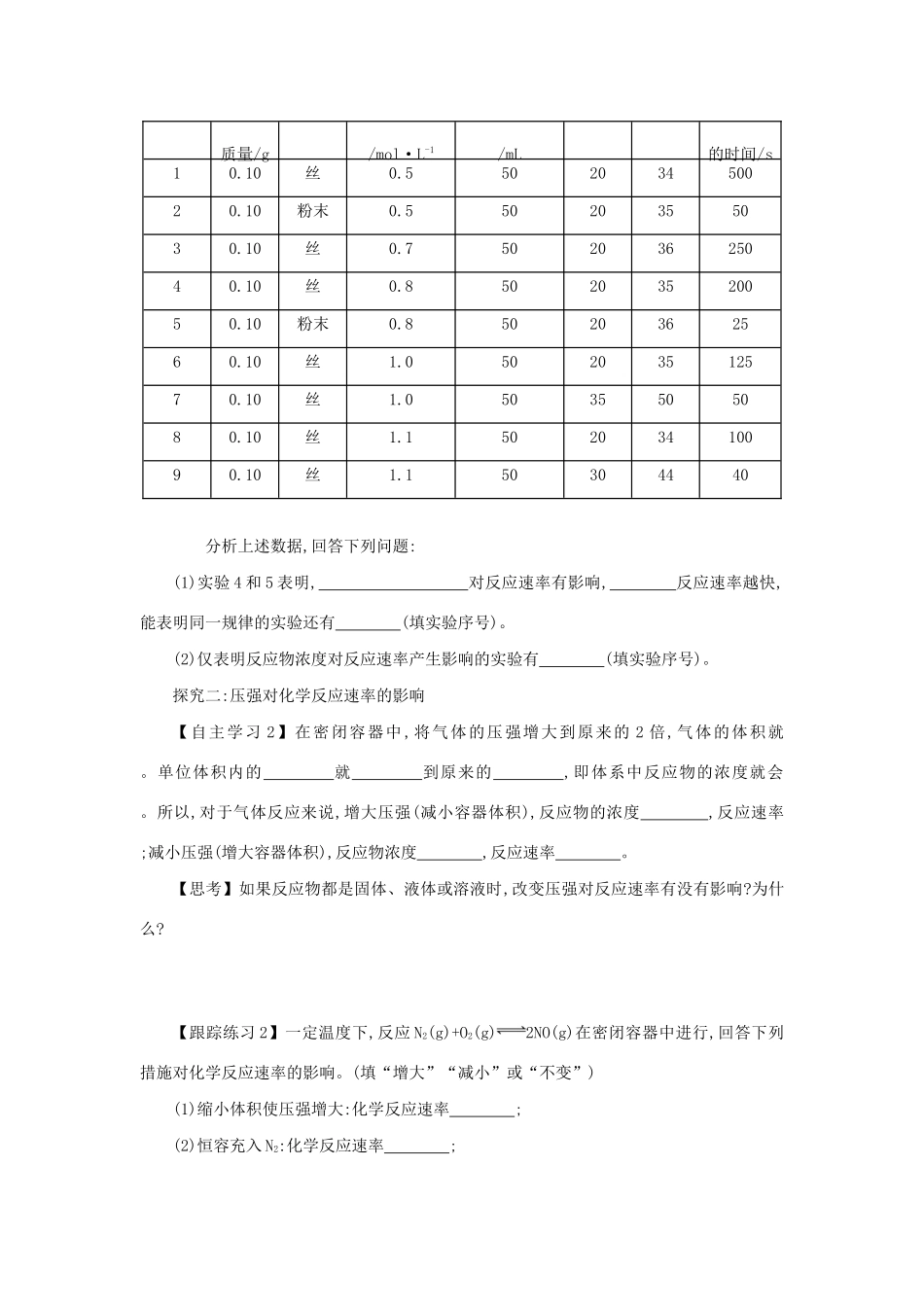
【跟踪练习1】下表是稀硫酸与某金属反应的实验数据:实验序号金属金属状态c(H2SO4)v(H2SO4)溶液温度/℃金属消失反应前反应后质量/g/mol·L-1/mL的时间/s10
550203450020
55020355030
750203625040
850203520050
85020362560
050203512570
05035505080
150203410090
150304440分析上述数据,回答下列问题:(1)实验4和5表明,对反应速率有影