课题:第三节电解池【学习目标】知道电解在氯碱工业、电镀、电冶金方面的应用【学习重点、难点】电解池的工作原理的应用【温习旧知】装置原电池电解池实例原理形成条件电极名称电子流向电流流向电极反应能量转化应用【学习新知】二、电解原理的应用1
电解食盐水【思考】(1)通电前,饱和食盐水中存在哪些离子
这些离子的运动情况怎样
(2)在电解装置中可否选用铜作阴、阳极的电极材料,为什么
(3)通电后,溶液中的离子运动发生了什么变化
(4)通电后,溶液中的在阴、阳放电的是什么离子
(5)电解后,在阴极区和阳极区分别得到的产物是什么
怎样初步检验两极产物的生成
【知识总结】电解食盐水阳极:阴极:总式:电解饱和食盐水可以制造
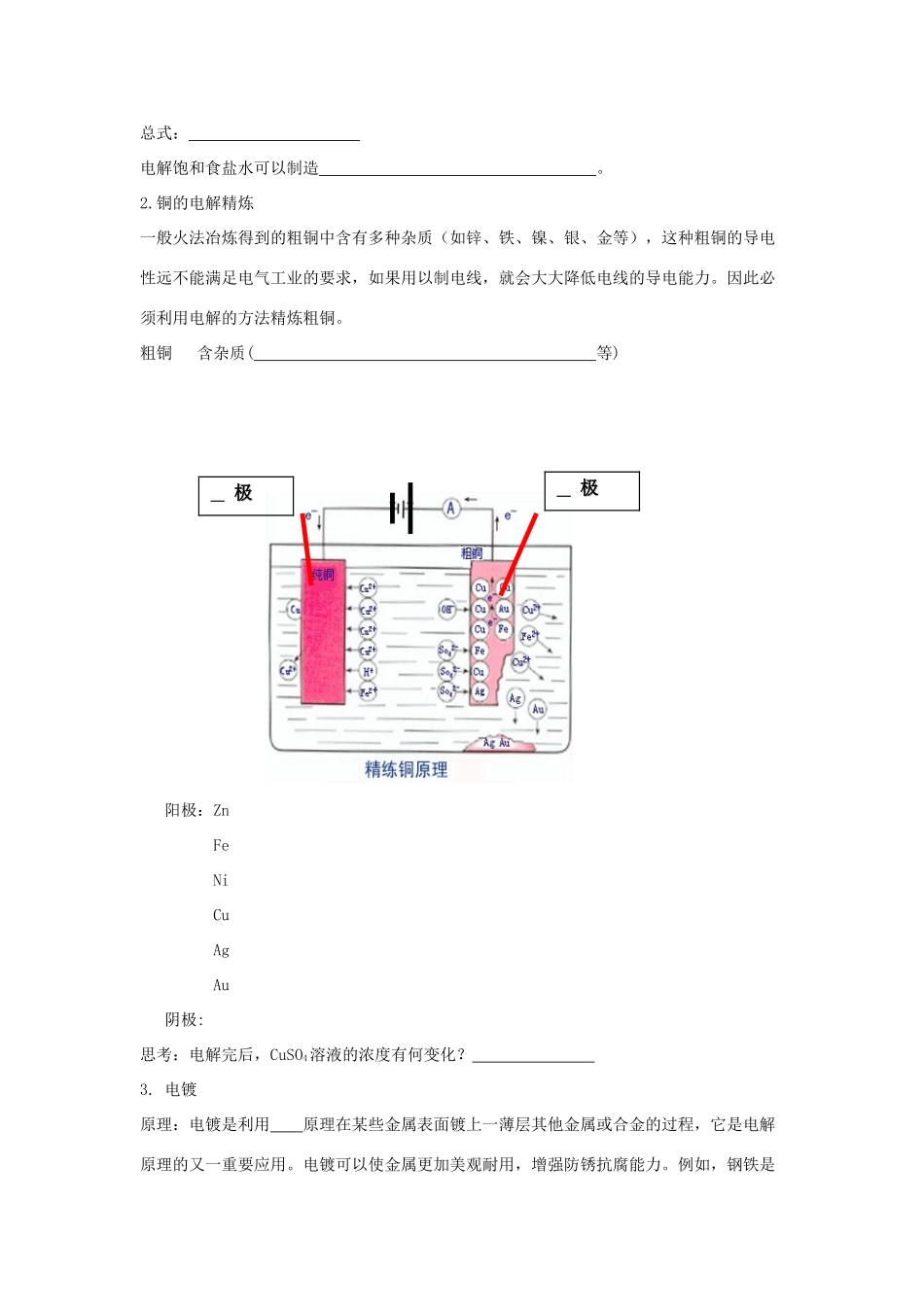
铜的电解精炼一般火法冶炼得到的粗铜中含有多种杂质(如锌、铁、镍、银、金等),这种粗铜的导电性远不能满足电气工业的要求,如果用以制电线,就会大大降低电线的导电能力
因此必须利用电解的方法精炼粗铜
粗铜含杂质(等)阳极:ZnFeNiCuAgAu阴极:思考:电解完后,CuSO4溶液的浓度有何变化
电镀原理:电镀是利用原理在某些金属表面镀上一薄层其他金属或合金的过程,它是电解原理的又一重要应用
电镀可以使金属更加美观耐用,增强防锈抗腐能力
例如,钢铁是极极极极人们最常用的金属,但钢铁有个致命的缺点,就是它们易被腐蚀
防止钢铁发生腐蚀的一种最常用方法就是在其表面镀上其他金属,如锌、铜、铬、镍等
①电极:阳极——金属或惰性电极阴极——金属制品②电镀液:含有金属离子的电解质溶液
溶液中CuSO4的浓度保持或4、电冶金制取金属钠←电解熔融状态的氯化钠
阳极:阴极:总反应:冶炼铝原理:阳极:阴极:总式:助熔剂:冰晶石(Na3AlF6六氟合铝酸钠)【思考】工业上为什么用电解熔融氧化铝的方法冶炼铝而不用AlCl3
【思考与交流】试比较电解饱和食盐水与电解熔融氯化钠的异同((提示提示::比