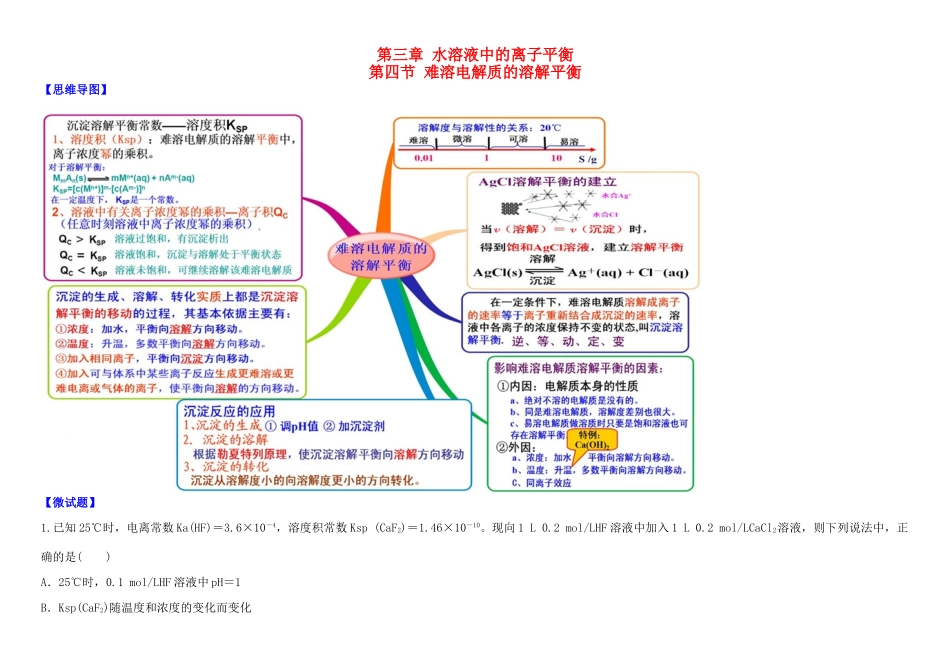
第三章水溶液中的离子平衡第四节难溶电解质的溶解平衡【思维导图】【微试题】1
已知25℃时,电离常数Ka(HF)=3
6×10-4,溶度积常数Ksp(CaF2)=1
46×10-10
2mol/LHF溶液中加入1L0
2mol/LCaCl2溶液,则下列说法中,正确的是()A.25℃时,0
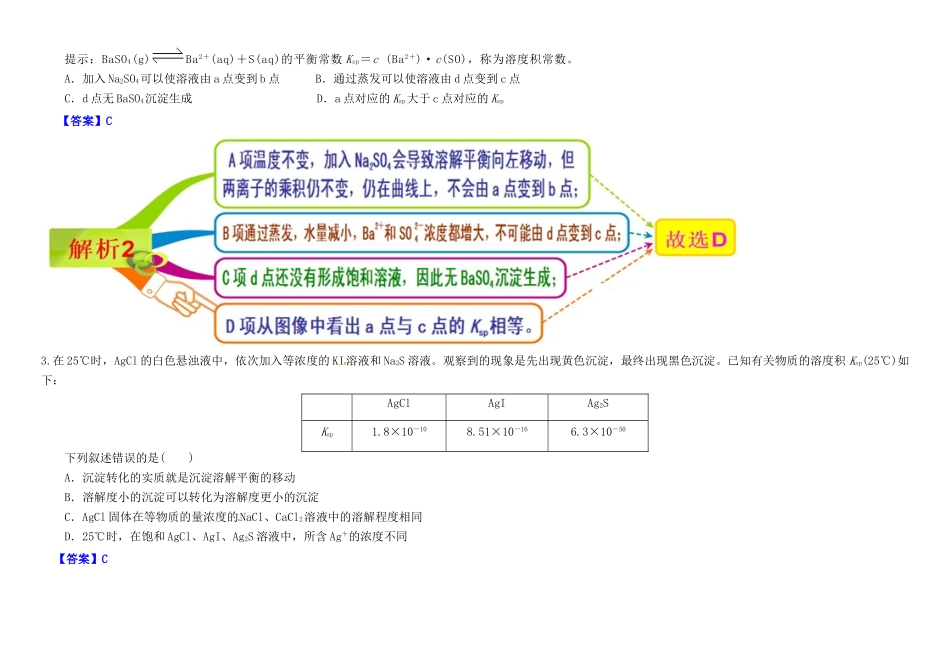
1mol/LHF溶液中pH=1B.Ksp(CaF2)随温度和浓度的变化而变化C.该体系中没有沉淀产生D.该体系中HF与CaCl2反应产生沉淀【答案】D2
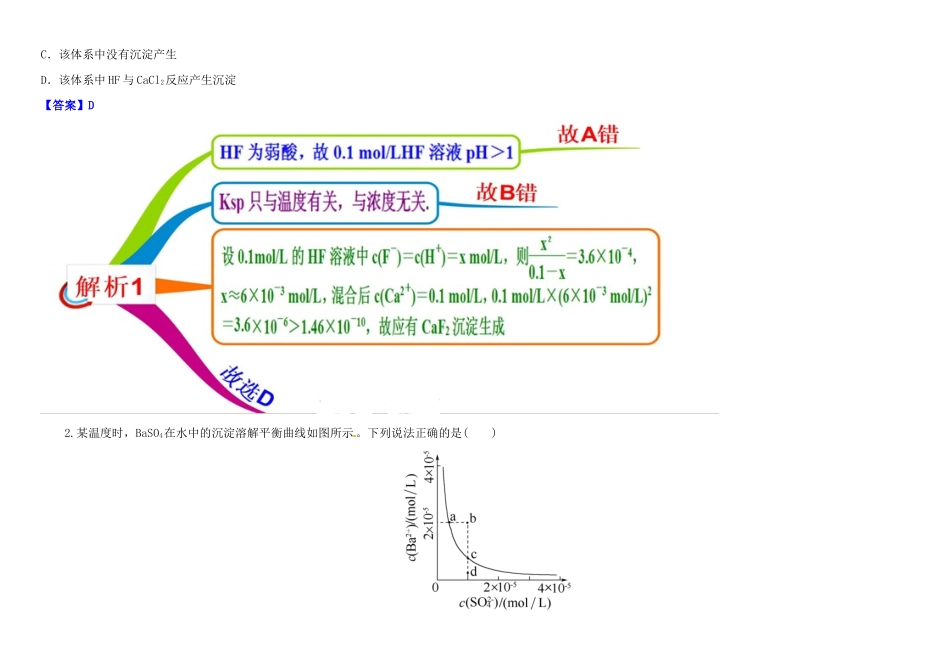
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示
下列说法正确的是()提示:BaSO4(g)Ba2+(aq)+S(aq)的平衡常数Ksp=c(Ba2+)·c(SO),称为溶度积常数
A.加入Na2SO4可以使溶液由a点变到b点B.通过蒸发可以使溶液由d点变到c点C.d点无BaSO4沉淀生成D.a点对应的Ksp大于c点对应的Ksp【答案】C3
在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液
观察到的现象是先出现黄色沉淀,最终出现黑色沉淀
已知有关物质的溶度积Ksp(25℃)如下:AgClAgIAg2SKsp1
8×10-108
51×10-166
3×10-50下列叙述错误的是()A.沉淀转化的实质就是沉淀溶解平衡的移动B.溶解度小的沉淀可以转化为溶解度更小的沉淀C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同【答案】C4
(2012·海南高考)在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:I:向废液中投入过量铁屑,充分反应后分离出固体和滤液:II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气
己知:Ksp[Fe(OH)3]=4
0×10-38回答下列问题