三、硝酸的性质11
物理性质(1)纯HNO3是色、易,有气味的液体
挥发刺激性无(2)能与水任意比互溶
常用浓硝酸质量分数为69%
质量分数为98%以上的硝酸为“发烟硝酸”
(3)纯HNO3的沸点是83℃,密度为1
5027g/cm3,22
化学性质(1)酸的通性:1
使紫色的石蕊试液变红;2
与金属反应,但不产生氢气;3
与某些金属氧化物起反应;2HNO3+CuO=Cu(NO3)2+H2O4
与碱起反应HNO3+NaOH=NaNO3+H2O5
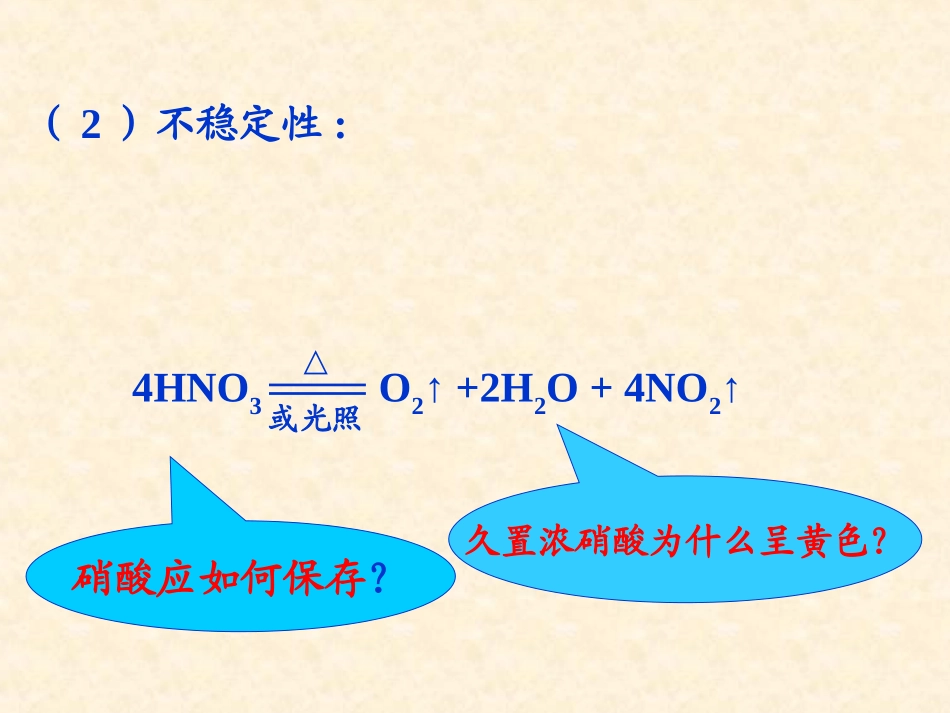
与某些盐起反应2HNO3+CaCO3=Ca(NO3)2+CO2↑+H2O(2)不稳定性:4HNO3O2↑+2H2O+4NO2↑△或光照硝酸应如何保存
久置浓硝酸为什么呈黄色
4HNO3O2↑+2H2O+4NO2↑△或光照久置硝酸分解产生的NO2溶于溶液中,使得溶液变黄
密封于棕色瓶中,并放在阴暗处
保存:(3)强氧化性:实验现象:实验结论:实验操作:溶液中有气泡产生,具支试管中充满红棕色气体,小试管中为无色气体
NO32HNOO2H23NOCu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O(3)强氧化性:实验现象:实验结论:实验操作:溶液中有气泡产生,具支试管、小试管中气体均为无色
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O【发散思维】【发散思维】•试推测常温下,浓硝酸、稀硝酸与不活泼金属银的反应方程式
Ag+2HNO3(浓)=AgNO3+NO2↑+H2O3Ag+4HNO3(稀)=3AgNO3+NO↑+2H2O(3)强氧化性:②②硝酸能与许多非金属反硝酸能与许多非金属反应应::C+4HNO3(浓)CO2↑+4NO2↑+2H2O③③硝酸能与许多还原性化合物反硝酸能与许多还原性化合物反应应::如如:SO:SO22、、NaNa22SOSO33、、KIKI、、FeClFeCl22等