影响化学平衡的条件【复习】化学平衡状态的定义:一定条件下,可逆反应里,正反应速率和逆反应速率相等,反应混合物中各组分的浓度保持不变的状态
化学平衡的特征:逆等动定变——可逆反应(或可逆过程)——V正=V逆(不同的平衡对应不同的速率)——动态平衡
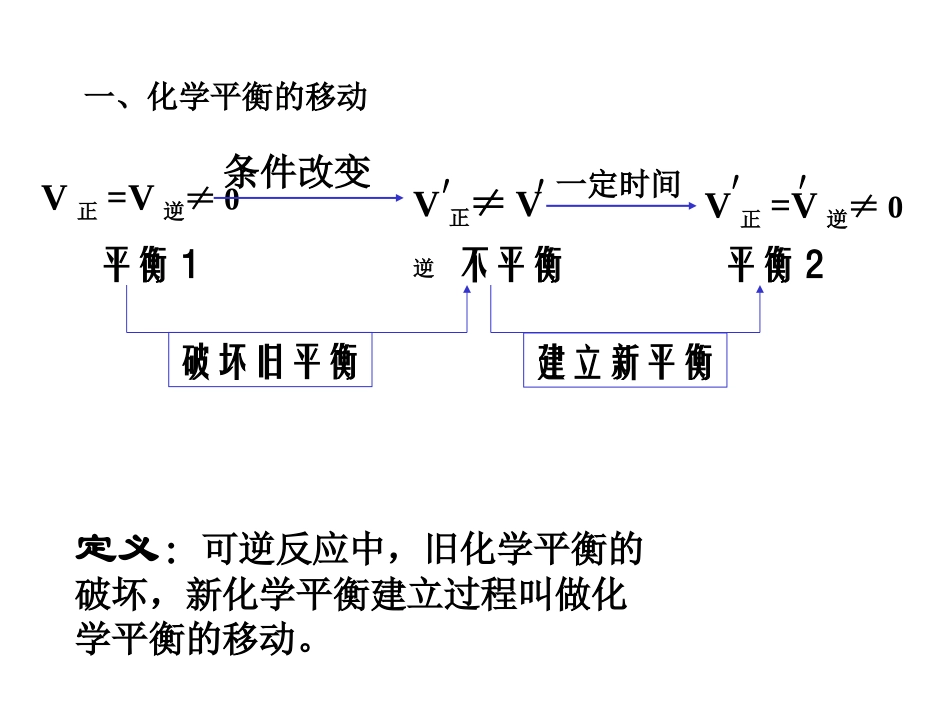
达平衡后,正逆反应仍在进行(V正=V逆≠0)——平衡时,各组分浓度、含量保持不变(恒定)——条件改变,平衡发生改变定义:可逆反应中,旧化学平衡的破坏,新化学平衡建立过程叫做化学平衡的移动
V正≠V逆V正=V逆≠0条件改变平衡1不平衡平衡2建立新平衡破坏旧平衡V正=V逆≠0′′化学平衡的移动一定时间一、化学平衡的移动′′条件改变自发新平衡V”正=V”逆V正=V逆原平衡V’正≠V’逆原平衡被破坏浓度、温度、压强发生改变“自发”的特点
新平衡与旧平衡的改变
二影响化学平衡的条件浓度温度压强化学平衡的前提:实质:标志:一定条件、可逆反应V正=V逆不等于0反应混合物中各组分浓度保持不变
1浓度对化学平衡的影响:实验:两试管中各加入5ml0
1mol/LK2Cr2O7溶液,按要求操作,观察颜色的变化
滴加3~10滴浓硫酸滴加10~20滴6mol/LNaOHK2Cr2O7溶液橙色黄色讨论:增大或减小生成物的浓度,平衡怎样移动
编号K2Cr2O7溶液现象原因结论1号试管3-10滴浓硫酸2号试管10-20滴6mol/L的NaOH溶液Cr2O72-(橙色)+H2O2CrO42-(黄色)+2H+Cr2O72-的浓度增大了橙色变深黄色变深增大C生,平衡逆向移动减小C生,平衡正向移动实验2:已知在已知在KK22CrCr22OO77的溶液中存在着如下平衡:的溶液中存在着如下平衡:CrO42-的浓度增大了[探究汇报]现象分析:Cr2O72-+H2O2CrO42-+2H+橙色黄色滴加3~10滴浓H2SO4滴加10~20滴6mol/LNaOHK2Cr2O7溶液增大