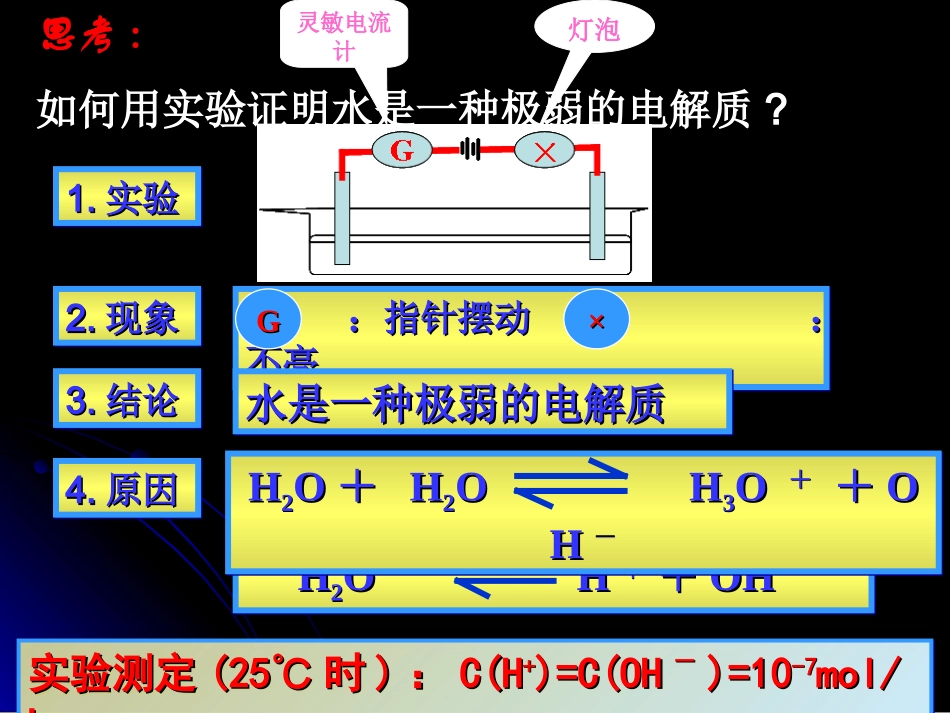
第三章水溶液中的离子平衡第三章水溶液中的离子平衡人教版选修4·化学反应原理22水的电离和溶液的酸碱性水的电离和溶液的酸碱性思考思考::如何用实验证明水是一种极弱的电解质
现象现象:指针摆动::指针摆动:不亮不亮:指针摆动::指针摆动:不亮不亮GG××3
结论结论水是一种极弱的电解质水是一种极弱的电解质水是一种极弱的电解质水是一种极弱的电解质4
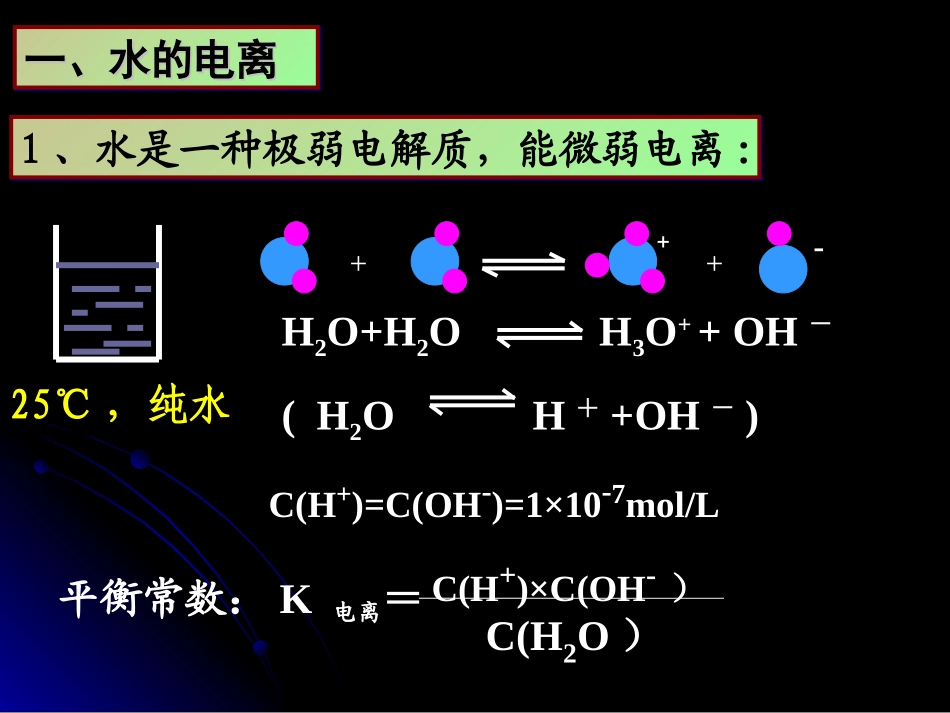
原因原因HH22OHOH++++OHOH--HH22OHOH++++OHOH--HH22OO++HH22OHOH33OO++++OOHH--HH22OO++HH22OHOH33OO++++OOHH--实验测定实验测定(25℃(25℃时时))::C(HC(H++)=C(OH)=C(OH--)=10)=10-7-7mol/mol/LL实验测定实验测定(25℃(25℃时时))::C(HC(H++)=C(OH)=C(OH--)=10)=10-7-7mol/mol/LL灵敏电流计灯泡25℃,纯水H2O+H2OH3O++OH-(H2OH++OH-)C(H+)=C(OH-)=1×10-7mol/L平衡常数:K电离=C(H+)×C(OH-)C(H2O)一、水的电离一、水的电离一、水的电离一、水的电离+++-1、水是一种极弱电解质,能微弱电离:1、水是一种极弱电解质,能微弱电离:Kw=c(H+)
c(OH-)1)表达式:KW叫做水的离子积常数,简称水的离子积
在任何水溶液中,均存在水的电离平衡,也就是任何水溶液中都是H+、OH-共存的
任何水溶液中都存在Kw=c(H+)
c(OH-)水的浓度为常数,所以C(H+)×C(OH-)=K电离
C(H2O)=常数2、水的离子积常数2、水的离子积常数注:提问:根据前面所学知识,水的离子积会受什么外界条件影响