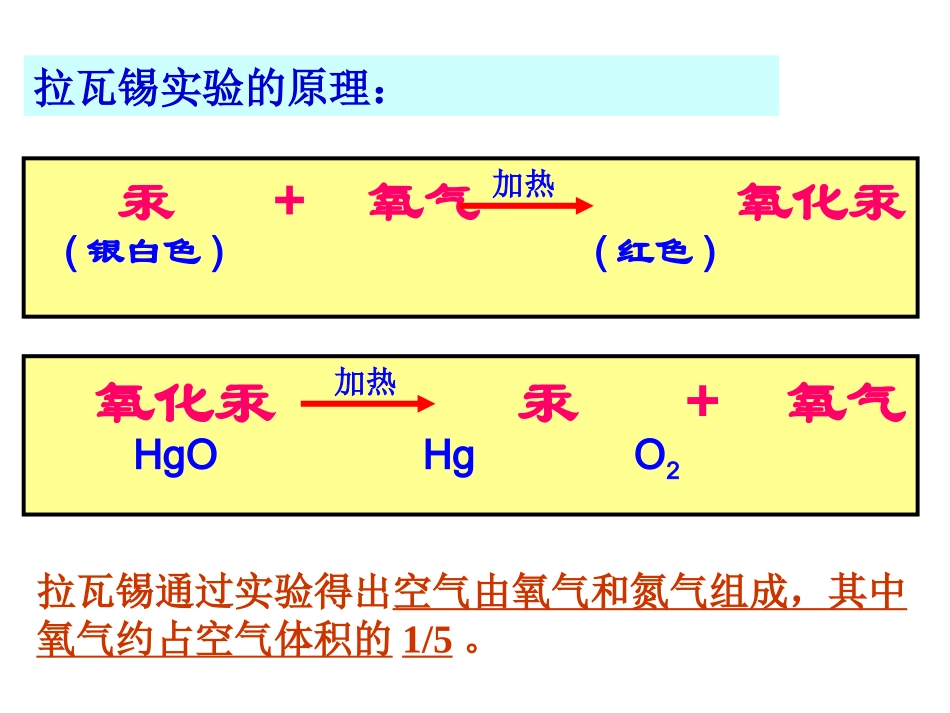
课题1空气我们周围的空气拉瓦锡研究空气成分所用的装置一、法国化学家拉瓦锡的贡献拉瓦锡通过实验得出空气由氧气和氮气组成知识点一、空气是由什么组成的拉瓦锡实验的原理:汞+氧气氧化汞(银白色)(红色)加热氧化汞汞+氧气HgOHgO2加热拉瓦锡通过实验得出空气由氧气和氮气组成,其中氧气约占空气体积的1/5
二、测定空气中氧气的含量•仿照这个历史上著名实验的原理,我们来测定空气里氧气的含量•实验用品仪器:燃烧匙、酒精灯、玻璃钟罩药品:红磷PO2P2O5五氧化二磷点燃实验原理:红磷+氧气实验现象:1、红磷燃烧,发出黄色火焰,产生大量白烟;2、等到燃烧停止,冷却后,瓶内水面上升了约1/5体积实验结论:氧气约占空气总体积的1/5
测定氧气实验装置测定氧气实验装置红磷集气瓶燃烧匙止水夹导气管烧杯测定空气中的氧气问题与思考:1、集气瓶中先加少量水的作用
防止燃着的红磷溅在集气瓶上,使集气瓶炸B
吸收生成的白烟五氧化二磷同时降温2、为什么点燃的红磷在伸入集气瓶中要迅速
红磷燃烧放出热量,部分空气会受热逸出(扩散),(导致进入水的体积大于1/5)
3、为什么要冷却后才打开止水夹
•因为温度高时,气体体积膨胀,压强大,而使进入集气瓶内的水的体积减少,从而造成实验结果偏小4、集气瓶内剩余气体主要成分是什么
它具有什么性质
N2,不溶于水,不支持燃烧5、能否用木炭(C)、硫(s)、细铁丝(Fe)代替红磷
不能,因为木炭和硫分别与氧气反应后,生成物都是气体,密闭容器内的压强几乎不变,因而不能使水进入集气瓶中,也就无法测出空气中氧气的含量,而铁丝在空气中不能燃烧,它只有在纯净的氧气中才燃烧
实验成功的关键:(1)装置不能漏气;(2)集气瓶中加少量水(防止高温熔融物使瓶底炸裂)(3)红磷应过量(4)点燃红磷后要立即伸入集气瓶中,并塞紧塞子(5)待红磷冷却后,打开弹簧夹2
用燃烧法测定空气中氧气的含