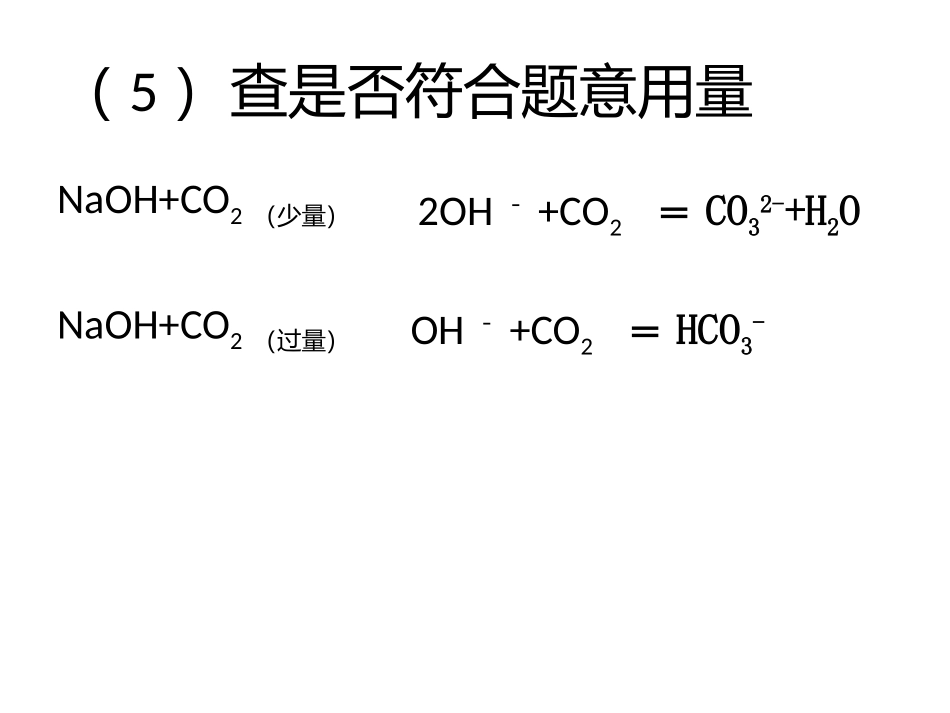
(5)查是否符合题意用量NaOH+CO2(少量)NaOH+CO2(过量)2OH-+CO2=CO32-+H2OOH-+CO2=HCO3-(6)注意实验的进程向NaHSO4溶液中逐滴加入Ba(OH)2至中性:中性后再加Ba(OH)2Ba2++2OH-+2H++SO42-=BaSO4↓+2H2OBa2++SO42-=BaSO4↓C、当反应物里有微溶物处于悬浊液或固态时,应写成化学式
例:在石灰乳中加入Na2CO3溶液:Ca(OH)2+CO32-=CaCO3↓+2OH-A、在生成物中有微溶物析出时,微溶物用化学式表示例:Na2SO4溶液中加入AgNO3溶液:SO42-+2Ag+=Ag2S04↓(7)对于微溶物:B、当反应物里有微溶物处于溶液状态(稀溶液),写成离子符号
例:CO2气体通入澄清石灰水中:CO2+Ca2++2OH-=CaCO3↓+H2OCa(OH)2(反应物)①澄清石灰水:拆为“Ca2+、OH-”②石灰乳或石灰浆:仍用“Ca(OH)2”氢氧化钙为生成物时,仍用“Ca(OH)2”
下列离子方程式正确的是()A、碳酸钙和稀盐酸反应CO32-+2H+=H2O+CO2↑B、铁和稀硫酸反应2Fe+6H+=2Fe3++3H2↑C、铝和硝酸铜溶液反应Al+Cu2+=Al3++CuD、碳酸钠和稀硫酸反应CO32-+2H+=CO2↑+H2O练习D四、离子共存问题1、溶液中离子不能共存的类型⑴生成难溶物或微溶物:如:Ba2+与CO32-、Ag+与Br-、Ca2+与SO42-等⑵生成气体或挥发性物质:如:NH4+与OH-,H+与CO32-、HCO3-、S2-、HS-、SO32-、HSO3-等⑶生成难电离物质:如:H+与Ac-、CO32-、S2-、SO32-等生成弱酸;OH-与NH4+生成的弱碱;H+与OH-生成水⑷发生氧化还原反应:氧化性离子(如Fe3+、NO3-、ClO-、MnO4-等与还