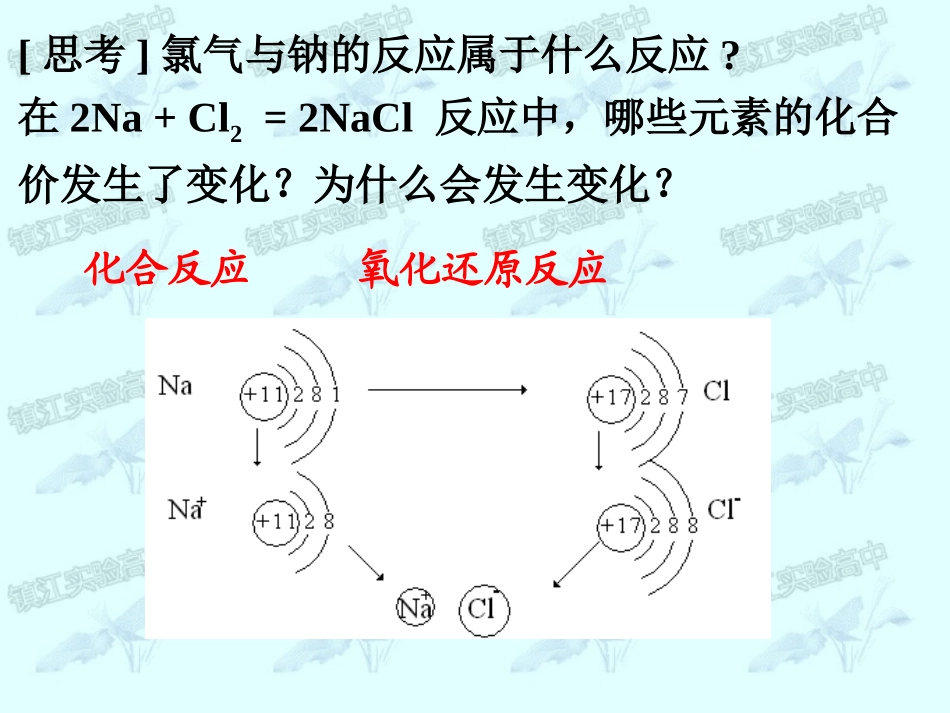
2-1-3氧化还原反应[思考]氯气与钠的反应属于什么反应
在2Na+Cl2=2NaCl反应中,哪些元素的化合价发生了变化
为什么会发生变化
化合反应氧化还原反应一、氧化还原反应1、定义:有电子转移的化学反应
(1)本质:电子转移(得失或偏移)
(2)特征:化合价改变
2、三组概念:(1)氧化剂和还原剂;(2)氧化性和还原性;(3)氧化反应和还原反应
3、还原剂:升、失、氧;氧化剂:降、得、还
还原剂:化合价升高失电子发生氧化反应氧化剂:化合价降低得电子发生还原反应(反应物)(特征)(本质)例1:在Fe2O3+3CO2Fe+3CO2的反应中,是氧化剂,是还原剂;具有氧化性,具有还原性;发生氧化反应,发生还原反应
二、电子转移的表示方法——双线桥法用箭头表示反应中同一元素的原子或离子得失电子的结果
1、标变价:首先标出变价元素的化合价
2、画箭号:用双箭号表示,箭号从反应物指向生成物且起止为同一元素
3、注得失:在箭号上要注明得电子、失电子的总数