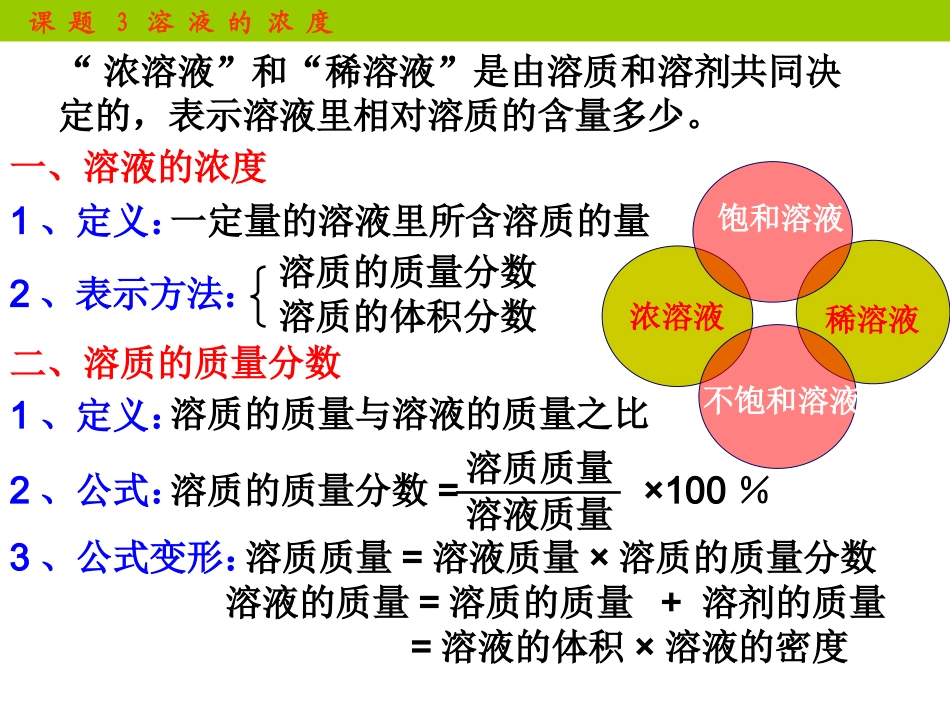
“浓溶液”和“稀溶液”是由溶质和溶剂共同决定的,表示溶液里相对溶质的含量多少
浓溶液稀溶液饱和溶液不饱和溶液一、溶液的浓度1、定义:溶质的质量分数溶质的体积分数溶质的质量分数=×100%溶质质量溶液质量二、溶质的质量分数3、公式变形:课题3溶液的浓度一定量的溶液里所含溶质的量2、表示方法:1、定义:溶质的质量与溶液的质量之比2、公式:溶质质量=溶液质量×溶质的质量分数溶液的质量=溶质的质量+溶剂的质量=溶液的体积×溶液的密度课题3溶液的浓度讨论:已知20℃时,氯化钠的溶解度是36g
有人说:“20℃时氯化钠饱和溶液中溶质的质量分数为36%
”这种说法对吗
20℃时,氯化钠的溶解度是36g
意思是:溶质质量36g,溶剂质量100g;溶液质量不是100g,而是100g+36g=136g
溶质的质量分数应为:36÷136×100%=26
5%练习:(课本P45)在20℃时,将40g硝酸钾固体加入100g水中,充分搅拌后,仍有8
4g硝酸钾固体未溶解
请填写下列空白:①所得溶液是20℃时硝酸钾的溶液;(填“饱和”或“不饱”)②20℃时硝酸钾的溶解度为;③所得溶液中硝酸钾的质量分数为
24%131
6g饱和实验室用100g稀硫酸和多少g锌恰好完全反应可制得0
H2SO4+Zn=ZnSO4+H29865100gx答:略A解:设所需锌的质量为xX65100g98x=66
3gH2SO4+Zn=ZnSO4+H2652x0
8gB解:设所需锌的质量为x0
8g2x65x=26g下面哪种解法正确
下面哪种解法正确
【解】溶液质量=溶液体积×溶液密度=500mL×1
1g/cm3=550g溶质质量=550g×10%=55g溶剂质量=550g—55g=495g答:需要氢氧化钠55g,水495g
课题3溶液的浓度练习:(课本P45)配制500mL质量分数为10%的氢氧