元素周期表3Li6
94111Na22
9919K39
1037Rb85
4755Cs132
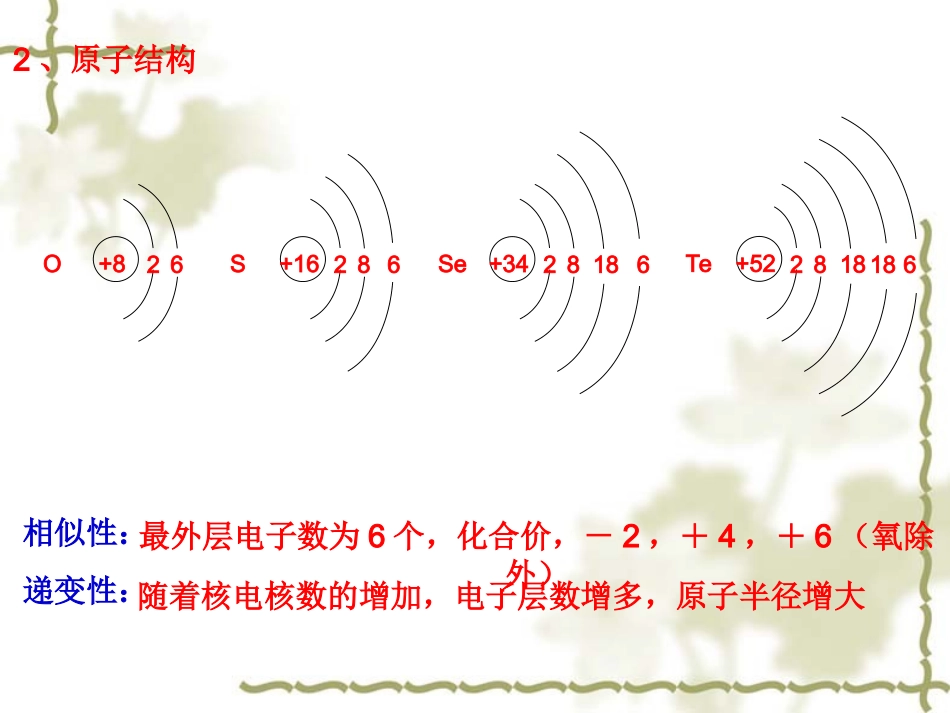
987Fr[223]OSSeTePo一、氧族元素1、位置2、原子结构+826O+1628S6+3428Se186+5228Te18186相似性:递变性:最外层电子数为6个,化合价,-2,+4,+6(氧除外)随着核电核数的增加,电子层数增多,原子半径增大3
氧族元素单质的化学性质元素名称和符号氧(O)硫(S)硒(Se)碲(Te)核电荷数8163452化合价-2(无正价)-2,+4,+6-2,+4,+6-2,+4,+6跟H2反应燃烧或爆炸加热时能化合加热时能化合不直接化合氢化物(H2X)的热稳定性很稳定,1000℃以上分解300℃以上分解不稳定,加热即分解不稳定,0℃即分解氧化物无SO2,SO3SeO2,SeO3TeO2,TeO3最高价氧化物的水化物无H2SO4H2SeO4H2TeO4,元素的非金属性稳定性:减弱非金属性减弱二、硫及其重要化合物的性质练习1、下列物质通过两种单质直接化合得()A、FeCl2B、FeSC、CuSD、Cu2SB、D单质硫与非金属、与金属反应(与变价金属反应时生成低价态的金属硫化物),说明硫的氧化性较弱
性质1、单质硫的性质H2SH2SO3SSO2SO3H2SO4Na2SO4FeSBaSO4⑴⑵⑶⑷⑸⑹⑺⑻⑼⑽⑾⑿⒀⒁练习2、把SO2通入下列物质a紫色石蕊b溴水cKMnO4d氢硫酸e品红f氢氧化钠(1)各装置的现象:___________________________________________________Br2+SO2+2H2O=2HBr+H2SO4(2)a、体现了SO2的________性b、中的化学反应为:________________________(3)c中体现SO2的____性(4)d、体现SO2______性
反应方程式为:_____