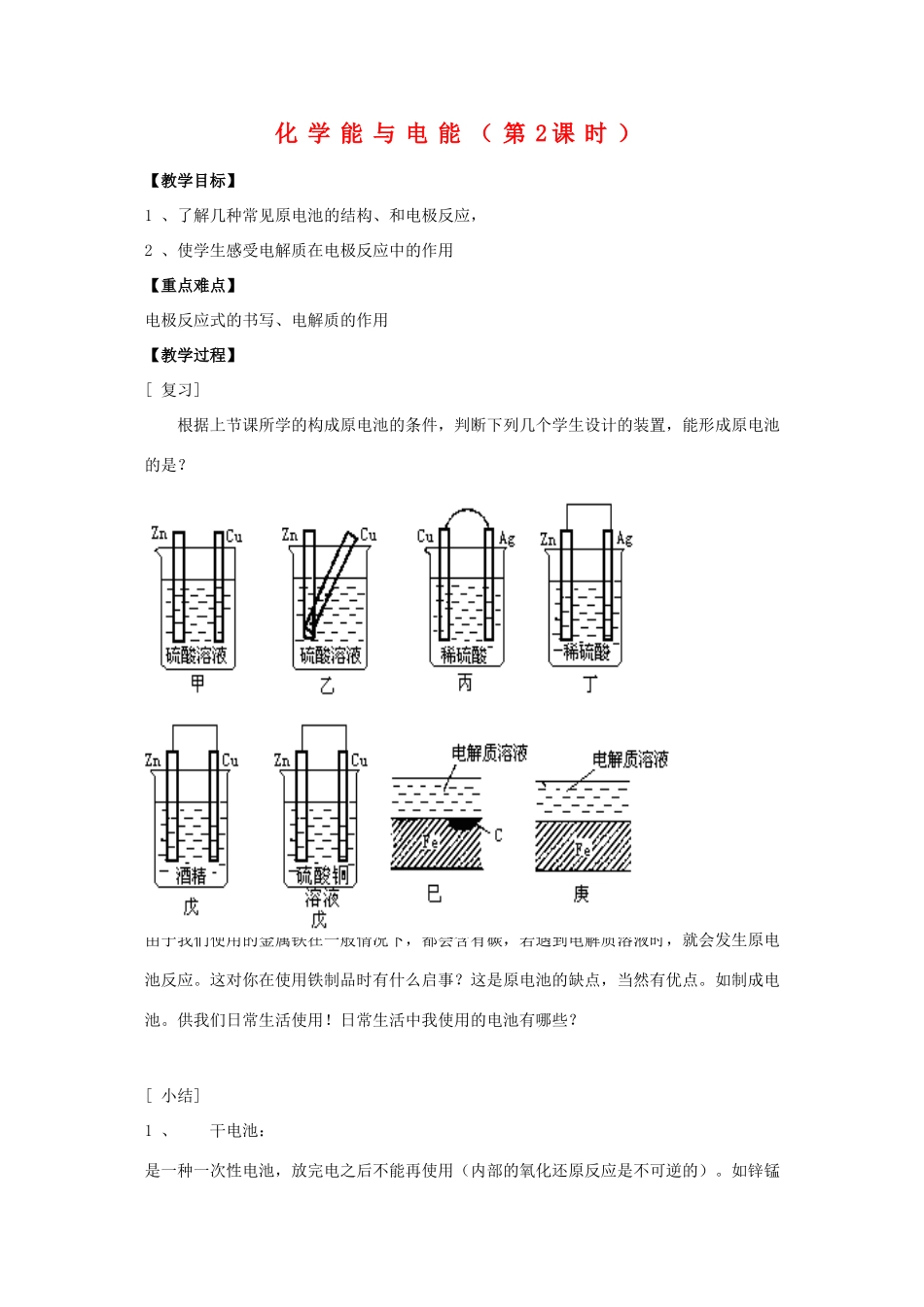
化学能与电能(第2课时)【教学目标】1、了解几种常见原电池的结构、和电极反应,2、使学生感受电解质在电极反应中的作用【重点难点】电极反应式的书写、电解质的作用【教学过程】[复习]根据上节课所学的构成原电池的条件,判断下列几个学生设计的装置,能形成原电池的是
[思考和交流]由于我们使用的金属铁在一般情况下,都会含有碳,若遇到电解质溶液时,就会发生原电池反应
这对你在使用铁制品时有什么启事
这是原电池的缺点,当然有优点
供我们日常生活使用
日常生活中我使用的电池有哪些
[小结]1、干电池:是一种一次性电池,放完电之后不能再使用(内部的氧化还原反应是不可逆的)
电极反应式为:负极(锌桶):正极(碳棒):2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O总反应:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O[学与问]锌锰干电池即使不用,放置过久,也可能会漏液失效(作为电解质的NH4Cl的水溶液显酸性),使用和保存时应注意什么
有时电池用时间久了会鼓起,为什么
[思考]如果电解质由NH4Cl换成KOH,那负极反应式该怎么写
这就是碱性干电池
换成KOH有什么好处
2、充电电池是一种可多次循环使用的电池
工作原理分为放电过程,和充电过程
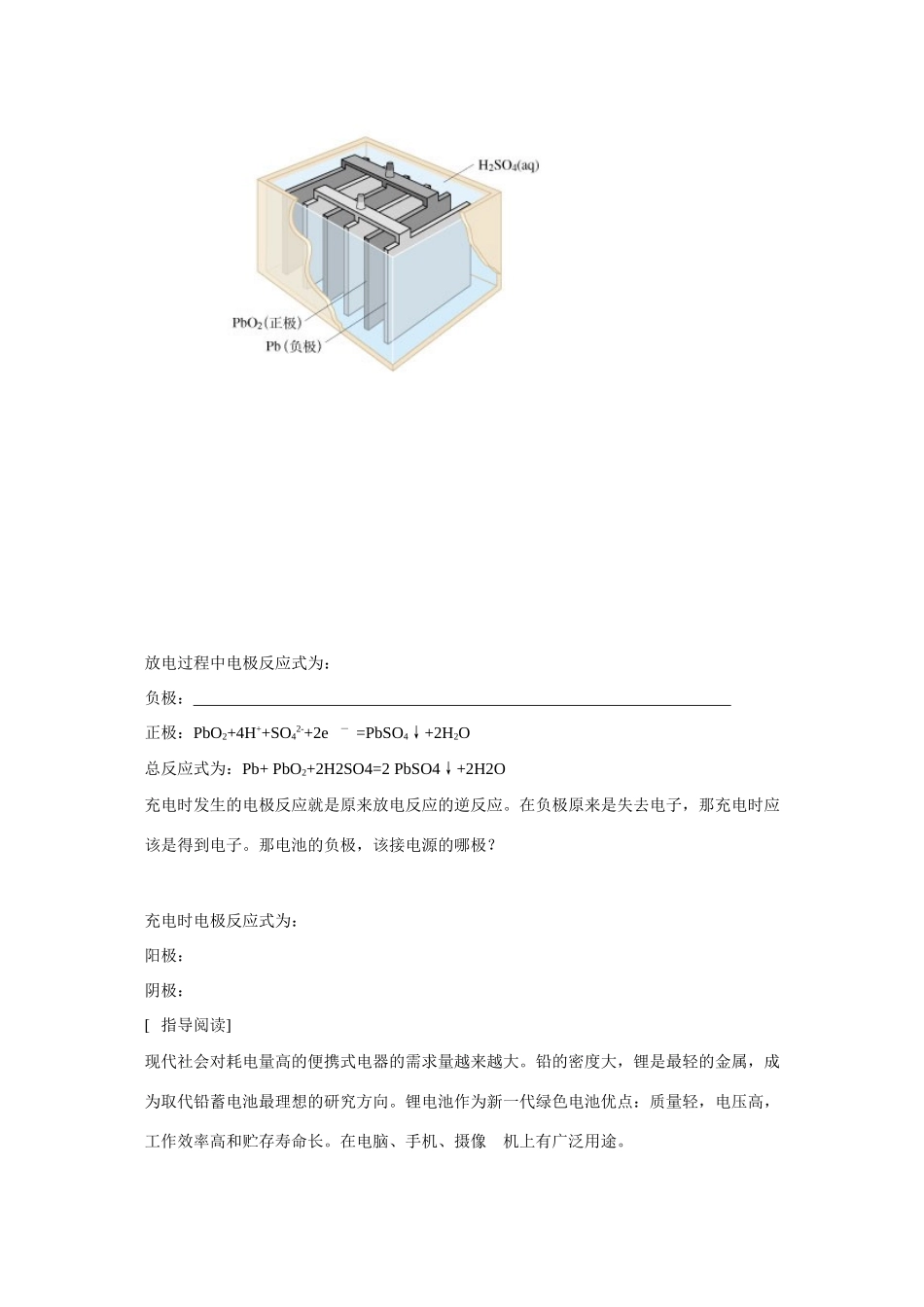
如广泛使用的铅蓄电池
构造如下放电过程中电极反应式为:负极:正极:PbO2+4H++SO42-+2e-=PbSO4↓+2H2O总反应式为:Pb+PbO2+2H2SO4=2PbSO4↓+2H2O充电时发生的电极反应就是原来放电反应的逆反应
在负极原来是失去电子,那充电时应该是得到电子
那电池的负极,该接电源的哪极
充电时电极反应式为:阳极:阴极:[指导阅读]现代社会对耗电量高的便携式电器的需求量越来越大
铅的密度大,锂是最轻的金属,成为取代铅蓄电池最理想的研究方向
锂电池作为新一代绿色电