第3节化学能转化为电能——电池考纲定位全国卷5年考情1
理解原电池的构成、工作原理及应用,能写出电极反应和总反应方程式
了解常见化学电源的种类及其工作原理
了解金属发生电化学腐蚀的原因、金属腐蚀的危害及保护措施
2017年:Ⅲ卷T112016年:Ⅱ卷T11;Ⅲ卷T112015年:Ⅰ卷T11;Ⅱ卷T26(1、2)2014年:Ⅱ卷T122013年:Ⅰ卷T10、T27(5)、T28(5);Ⅱ卷T11考点1|原电池及其工作原理(对应学生用书第121页)[考纲知识整合]1.原电池的概念把化学能转化为电能的装置,其本质是发生了氧化还原反应
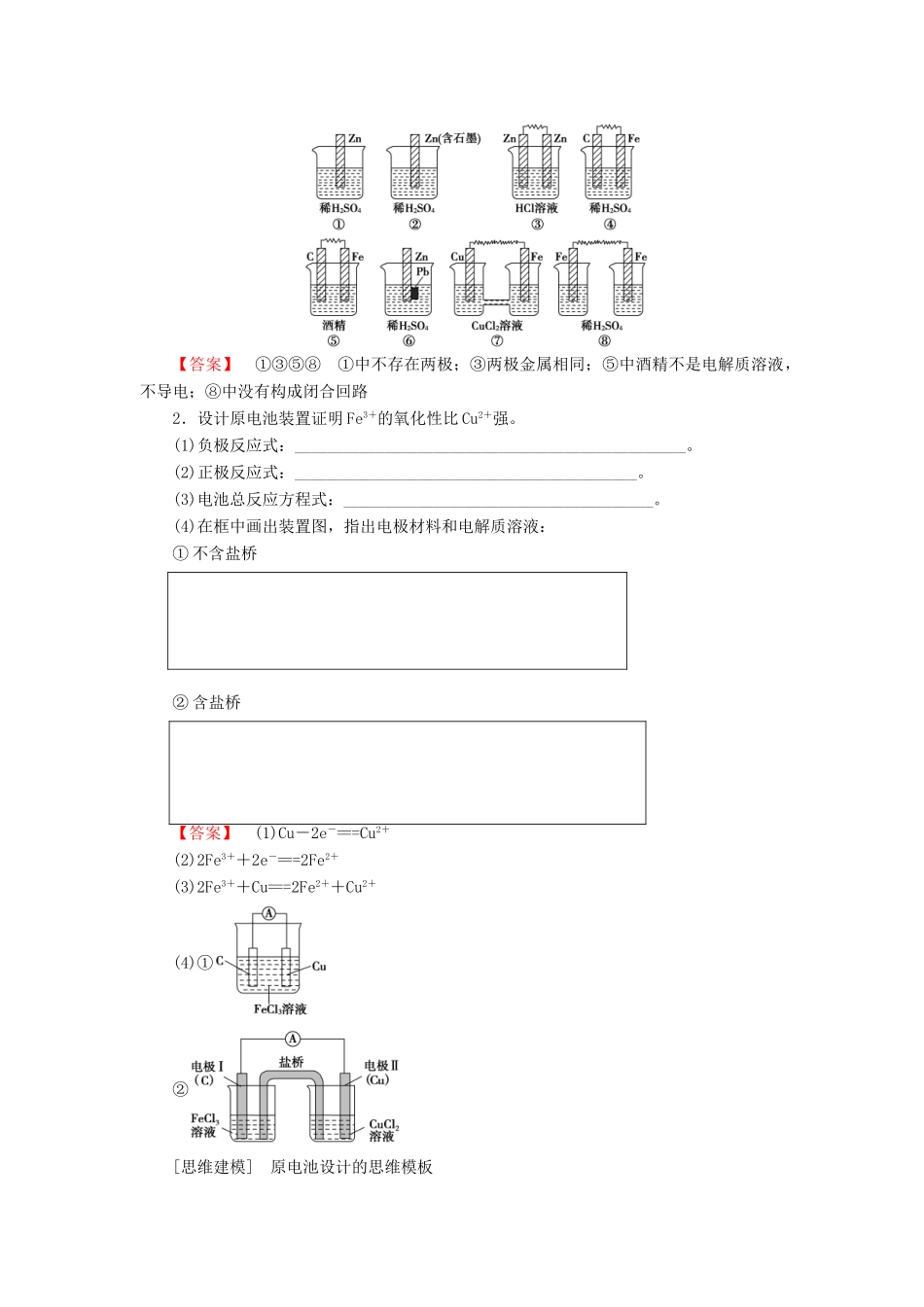
2.原电池的构成(1)有两个活动性不同的电极(常见为金属或石墨)
(2)将电极插入电解质溶液中
(3)两电极间构成闭合回路(两电极接触或用导线连接)
(4)能自发发生氧化还原反应
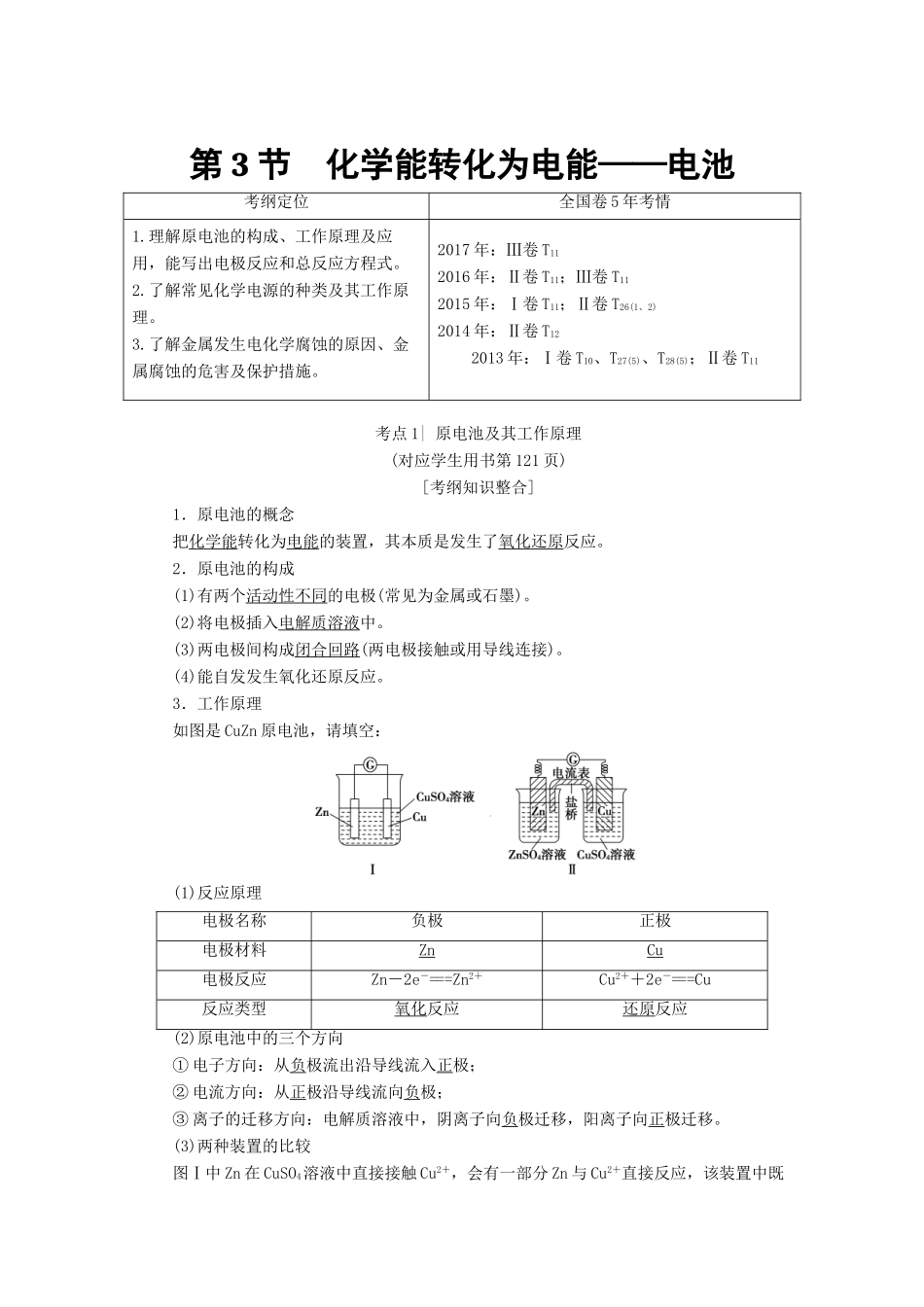
3.工作原理如图是CuZn原电池,请填空:(1)反应原理电极名称负极正极电极材料ZnCu电极反应Zn-2e-===Zn2+Cu2++2e-===Cu反应类型氧化反应还原反应(2)原电池中的三个方向①电子方向:从负极流出沿导线流入正极;②电流方向:从正极沿导线流向负极;③离子的迁移方向:电解质溶液中,阴离子向负极迁移,阳离子向正极迁移
(3)两种装置的比较图Ⅰ中Zn在CuSO4溶液中直接接触Cu2+,会有一部分Zn与Cu2+直接反应,该装置中既有化学能和电能的转化,又有一部分化学能转化成了热能,装置的温度会升高
图Ⅱ中Zn和CuSO4溶液分别在两个池中,Zn与Cu2+不直接接触,不存在Zn与Cu2+直接反应的过程,所以仅是化学能转化成了电能,电流稳定,且持续时间长
(4)盐桥作用①连接内电路,形成闭合回路;②平衡电荷,使溶液呈电中性,使原电池不断产生电流
4.原电池原理的三个应用(1)设计制作化学电源①首先将氧化还原反应分成两个半反应
②根据原电池的反应特点,结合两个