课时1电解原理及其规律目标与素养:1
了解电解池的构造和电解原理
(宏观辨识与变化观念)2
理解电解规律及电极反应和电解方程式的书写
(科学探究与模型认知)一、电解CuCl2溶液1.通电前,CuCl2溶液中存在的离子有Cu2+、Cl-、H+、OH-
2.工作原理(1)总反应:CuCl2=====Cu+Cl2↑
(2)电流方向:电源正极→阳极→阴极→电源负极
(3)电子流向:阳极→电源正极,电源负极→阴极
3.CuCl2溶液导电的过程就是CuCl2电解的过程,就是在阴、阳两极发生氧化还原反应的过程
二、电解和电解池1.电解的概念使电流通过电解质溶液而在阴、阳两极引起氧化还原反应的过程
2.电解装置——电解池(1)概念:将电能转变为化学能的装置
(2)构成条件①两个电极:阳极——与电源正极连接;阴极——与电源负极连接
②电解质溶液或熔融电解质
④构成闭合回路
(3)工作原理①电极反应类型阳极→氧化反应;阴极→还原反应
②电子流向:电源负极→阴极;阳极→电源正极
③电流方向:电源正极→阳极;阴极→电源负极
④离子流向:阳离子→阴极;阴离子→阳极
阴、阳离子在电解过程中的移动方向与在原电池中的移动方向有什么区别和联系
[答案]原电池中,阳离子移向正极;阴离子移向负极;电解池中,阳离子移向阴极;阴离子移向阳极
即阳离子都是移向发生还原反应的电极,阴离子都是移向发生氧化反应的电极
1.判断正误(正确的打“√”,错误的打“×”)(1)电解与电离均需要通电才可发生的
()(2)电解CuCl2溶液,Cu2+放电发生氧化反应
()(3)电解池的阳极与原电池的负极电极反应类型相同
()(4)电解过程中电子流向为负极→阴极→阳极→正极
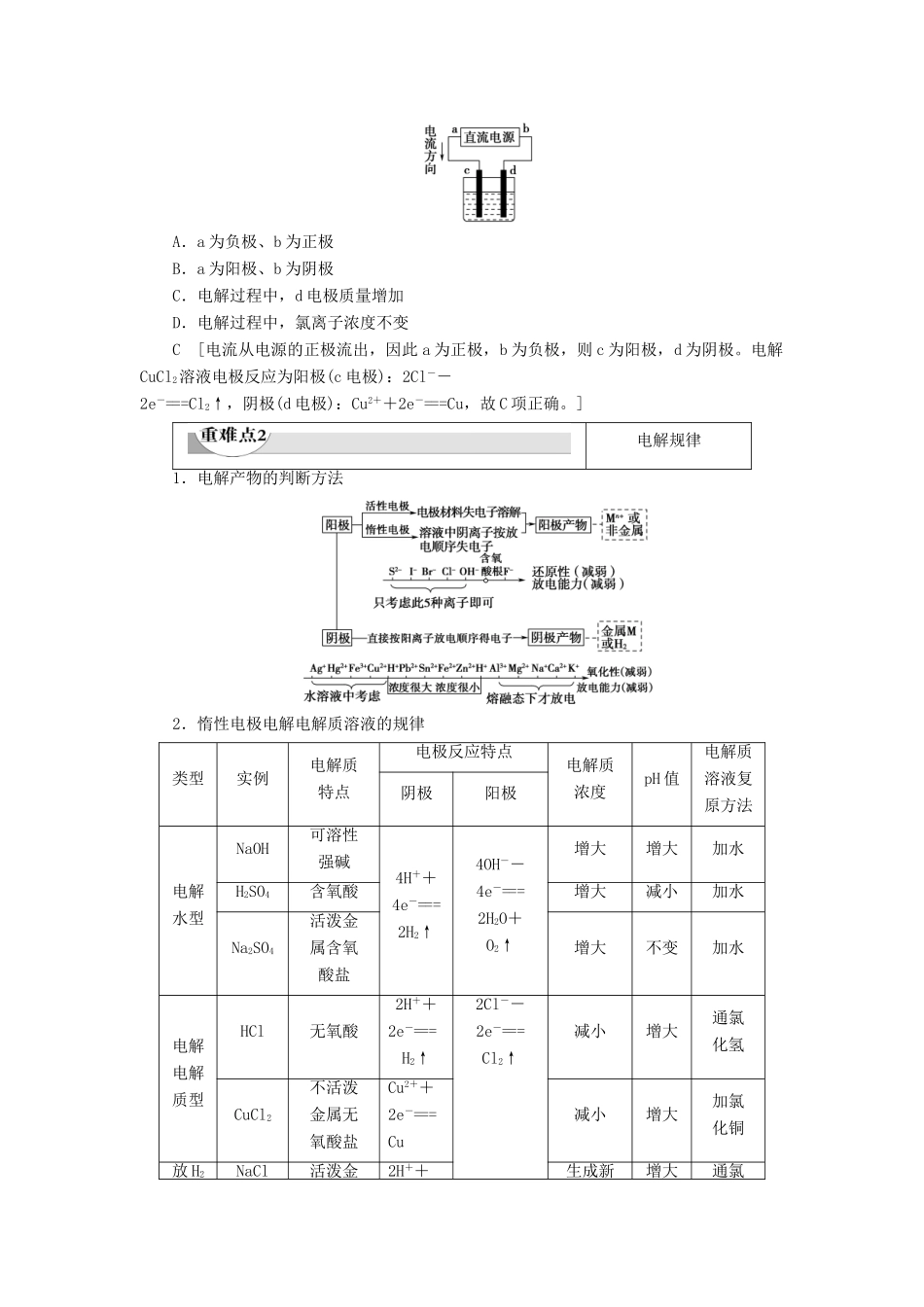
()[答案](1)×(2)×(3)√(4)×2.用石墨电极电解CuCl2溶液(见右图)
下列分析正确的是()A.a端是直流电源的负极B.通电使CuCl2