电解原理【学习目标】1、了解电解池的工作原理;2、初步掌握一般电解反应产物的判断方法
【要点梳理】要点一、电解原理1.定义:使电流通过电解质溶液(或熔融的电解质)而在阴、阳两极引起氧化还原反应的过程叫电解
2.装置特点:电能转化为化学能
3.形成条件:(1)与电源两个电极相连;(2)电解质溶液(或熔融的电解质);(3)形成闭合回路
4.阴阳极的判断及反应原理(以电解熔融NaCl、CuCl2溶液为例)【高清课堂:电解原理#电解反应类型】要点二、电解反应类型1.只有电解质参加的反应(电解CuCl2溶液)阳极:2Cl--2e-=Cl2↑(氧化反应)阴极:Cu2++2e-=Cu(还原反应)总反应:CuCl2Cu+Cl2↑2.只有水参加的反应(电解稀硫酸)阳极:4OH--4e-=2H2O+O2阴极:2H++2e-=H2总反应:2H2O2H2+O23.水和电解质均参加的反应(电解饱和食盐水)阳极:2Cl--2e-=Cl2阴极:2H++2e-=H2总反应:2NaCl+2H2OH2+Cl2+2NaOH4.电极参加的反应阳极反应:Cu-2e-=Cu2+阴极反应:2H+-2e-=H2总反应:Cu+2H+Cu2++H2要点三、电解时电极反应式的书写1.看电极
主要是看阳极是何类型的电极,若为活性电极,电极本身被氧化发生氧化反应
阴极一般不参与电极反应
搞清电解质溶液中存在哪些阴离子、阳离子,根据放电顺序书写电极反应式
3.水溶液中始终有H+和OH-,放电顺序中H+、OH-之后的离子一般不参与电极反应
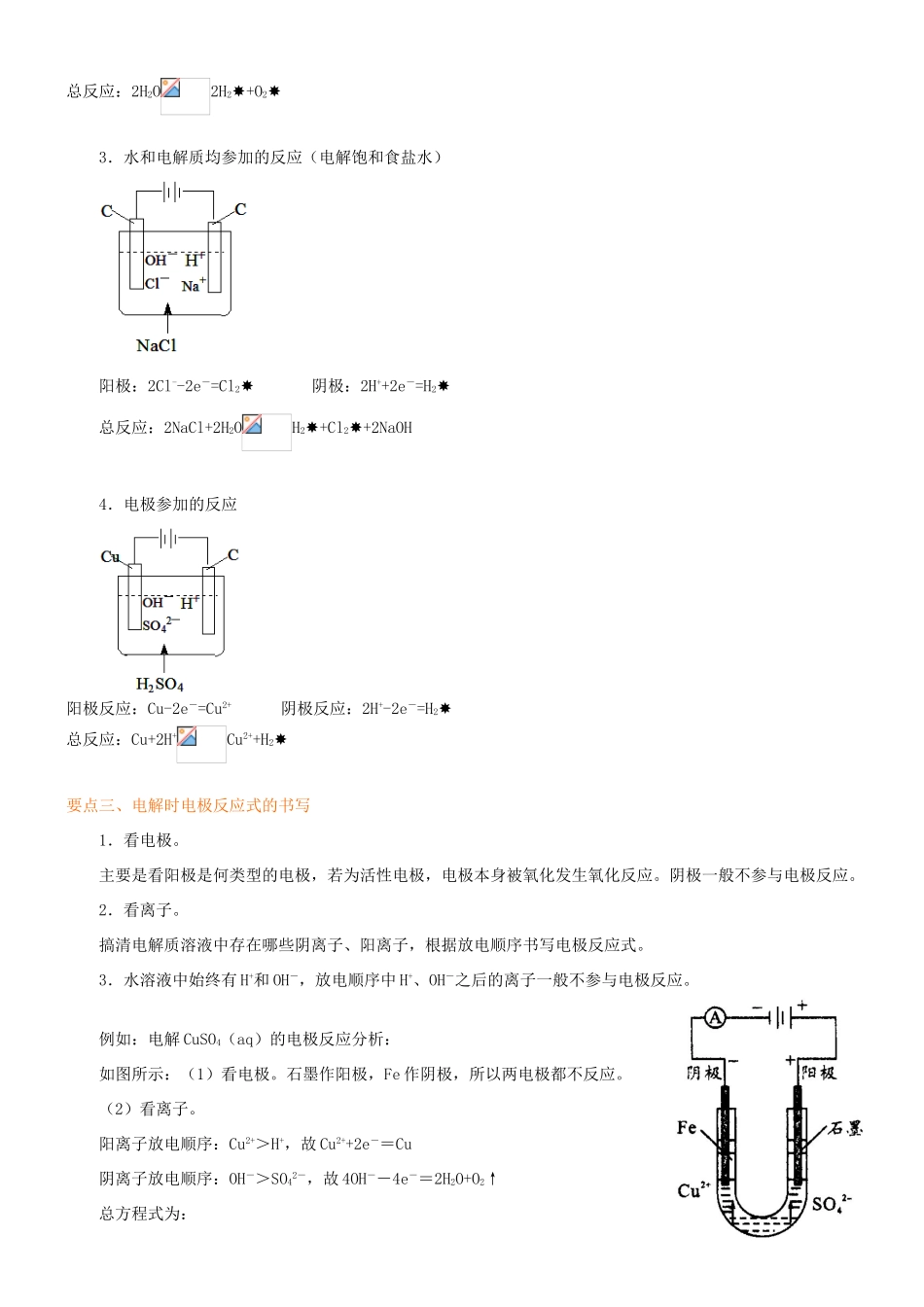
例如:电解CuSO4(aq)的电极反应分析:如图所示:(1)看电极
石墨作阳极,Fe作阴极,所以两电极都不反应
(2)看离子
阳离子放电顺序:Cu2+>H+,故Cu2++2e-=Cu阴离子放电顺序:OH->SO42-,故4OH--4e-=2H2O+O2↑总方程式为:2