第二节影响化学反应速率的因素1
理解外界条件(浓度、温度、压强、催化剂等)对化学反应速率的影响
了解催化剂在生产、生活和科研领域中的重大作用
知道活化能的含义及其对化学反应速率的影响
了解通过改变外界条件改变化学反应速率的方法和意义
浓度、压强对化学反应速率的影响一、活化分子与有效碰撞(绪言)1.有效碰撞(1)反应物分子间能发生反应的碰撞
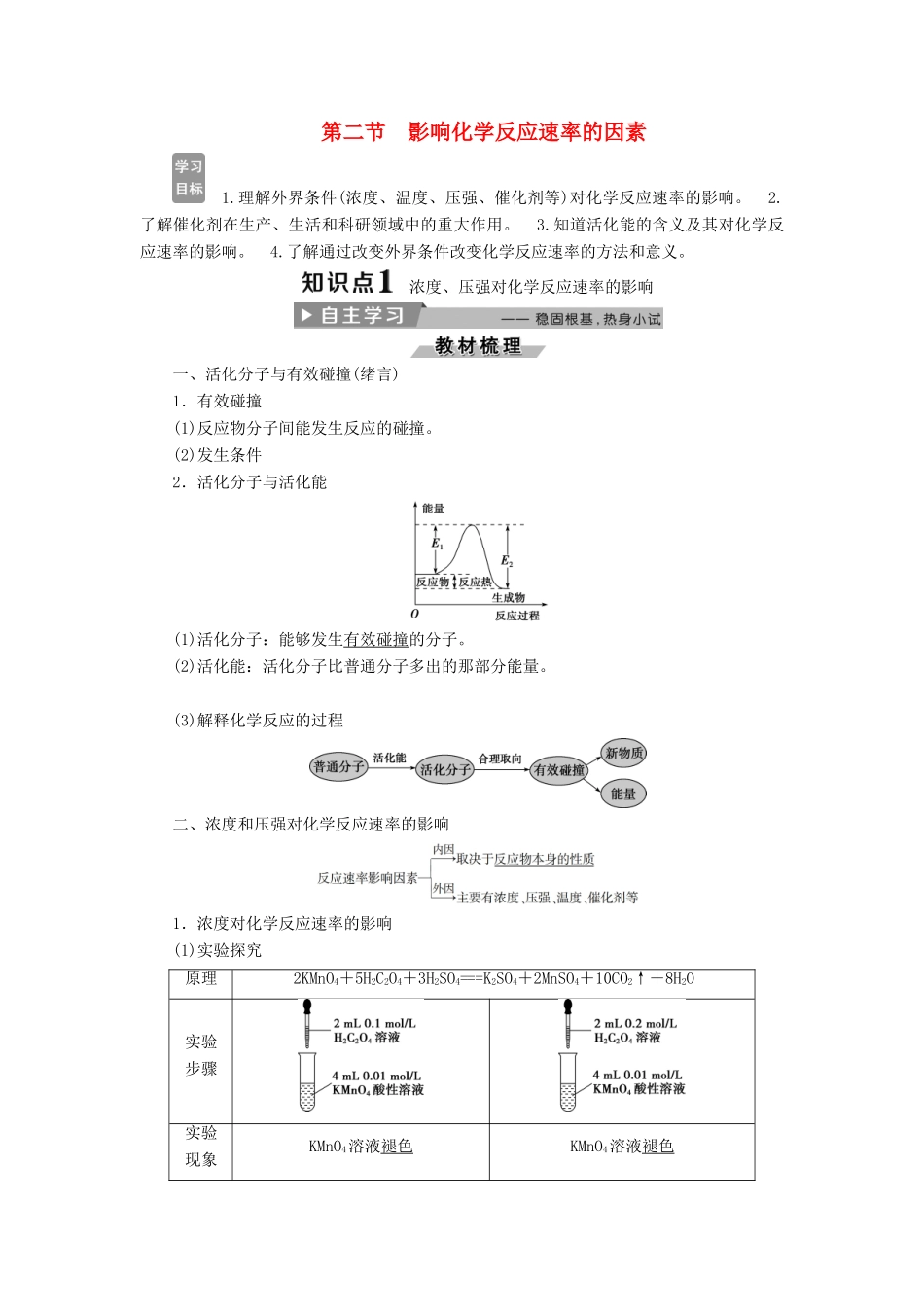
(2)发生条件2.活化分子与活化能(1)活化分子:能够发生有效碰撞的分子
(2)活化能:活化分子比普通分子多出的那部分能量
(3)解释化学反应的过程二、浓度和压强对化学反应速率的影响1.浓度对化学反应速率的影响(1)实验探究原理2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O实验步骤实验现象KMnO4溶液褪色KMnO4溶液褪色褪色时间加入0
2mol/LH2C2O4溶液比加入0
1mol/LH2C2O4溶液的试管中溶液褪色时间短结论若其他条件相同,H2C2O4浓度越大,KMnO4溶液褪色越快,反应速率也越快;反之,H2C2O4浓度越小,反应速率越慢(2)规律反应物浓度增大→反应速率加快;反应物浓度减小→反应速率减慢
(3)解释反应物浓度增大→单位体积内活化分子数增多→单位时间内有效碰撞次数增加→反应速率加快
2.压强对化学反应速率的影响(1)影响规律对于有气体参与的反应,在相同温度下,(2)微观解释对于有气体参与的反应,在相同温度下,增大压强→反应物浓度增大→反应速率加快;反之,减小压强→反应速率减慢
对于无气体参与的化学反应,改变压强对反应速率的影响可以忽略不计
1.判断正误(正确的打“√”,错误的打“×”)
(1)当碰撞的分子具有足够的能量和适当的取向时,才能发生化学反应
()(2)发生有效碰撞的分子一定是活化分子
()(3)活化分子间的碰撞一定是有效碰撞
()(4)活化分子