第二节元素周期律导学案(第2课时)【知识回顾】元素的金属性强弱判断依据
金属与酸或水的反应越容易,则元素金属性越
最高价氧化物对应的水化物碱性越强,元素的金属性越
同一周期越靠前,金属性越
同一主族越靠下,金属性越
4金属与盐溶液的置换反应A置换出B,则A元素金属性
5元素的金属性越,则对应金属单质的还原性越
【练习】下列叙述中,肯定a金属比b金属活泼性强的是()A.a原子的最外层电子数比B原子的最外层电子数少B.a原子电子层数比b原子的电子层数多C.1mola从酸中置换H+生成的H2比1molb从酸中置换H+生成的H2多D.常温时,A能从水中置换出氢,而B不能【教学过程】一、元素的非金属性强弱判断SiPSCl单质与氢气反应的条件磷蒸气与氢气能反应最高价氧化物对应的水化物(含氧酸)酸性强弱H2SiO3酸H3PO4酸H2SO4酸HClO4酸【总结]】元素的非金属性强弱判断依据:1非金属单质与氢化合越容易,则元素非金属性越
2形成的氢化物越稳定,则元素非金属性越
3最高价氧化物对应的水化物(含氧酸)酸性越强,则元素非金属性越
4同一周期越靠后,非金属性越
同一主族越靠上,非金属性越
5非金属元素之间的置换,A能置换出B,则A的非金属性
6元素的非金属性越,则对应非金属单质的氧化性越
【归纳小结】第三周期元素金属性逐渐,非金属性逐渐二、元素周期律(1)定义:
(2)实质:
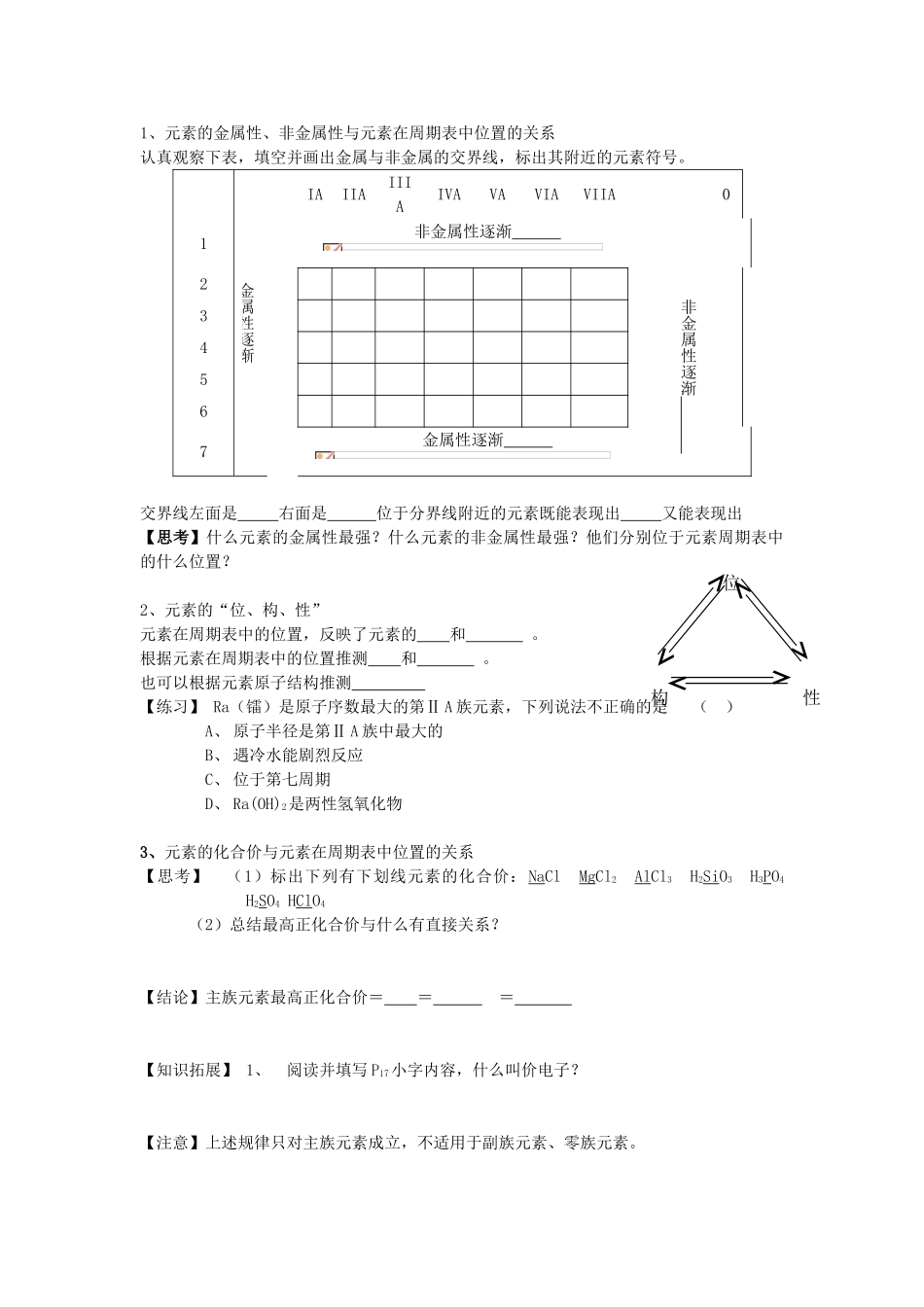
【练习】下列各组物质的性质变化正确的是()A.酸性HClO4>HNO3>H3PO4>H2SiO3B.稳定性H2S>HCl>HBr>HIC.熔点Pb>K>Na>LiD.溶解性NaHCO3>Na2CO3>NaOH三、元素周期表和元素周期律的应用1、元素的金属性、非金属性与元素在周期表中位置的关系认真观察下表,填空并画出金属与非金属的交界线,标出其附近的元素符号
金属性逐渐IAIIAIIIAIVAVAVI