复习:平衡的含义【复习】化学平衡状态的定义:一定条件下,可逆反应里,正反应速率和逆反应速率相等,反应混合物中各组分的浓度保持不变的状态
化学平衡的特征:逆等动定变——可逆反应(或可逆过程)——V正=V逆(不同的平衡对应不同的速率)——动态平衡
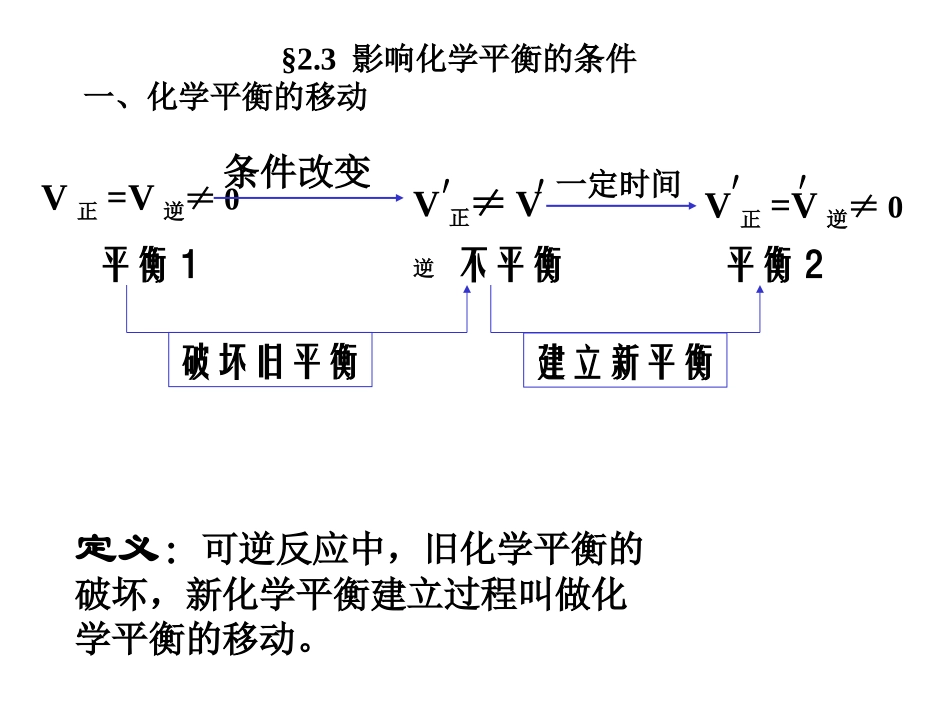
达平衡后,正逆反应仍在进行(V正=V逆≠0)——平衡时,各组分浓度、含量保持不变(恒定)——条件改变,平衡发生改变定义:可逆反应中,旧化学平衡的破坏,新化学平衡建立过程叫做化学平衡的移动
V正≠V逆V正=V逆≠0条件改变平衡1不平衡平衡2建立新平衡破坏旧平衡V正=V逆≠0′′化学平衡的移动一定时间§2
3影响化学平衡的条件一、化学平衡的移动′′影响化学平衡的条件浓度温度压强现有实验资源:药品:0
01mol/LFeCl3溶液、0
01mol/LKSCN溶液、1mol/LFeCl3溶液、1mol/LKSCN溶液
仪器:点滴板、小烧杯、充有NO2气体的连通球可供选择研究的可逆反应:反应一:FeCl3+3KSCNFe(SCN)3+3KCl黄色红色反应二:红棕色无色2NO2N2O4(正反应为放热反应)(g)(g)实验目的:研究了解浓度和温度这个两个条件对化学平衡的影响实验设计--讨论--确立方案--动手实验实验设计的关键•建立平衡体系•控制单个变量进行对照实验浓度对化学平衡的影响浓度对平衡的影响实验现象及分析:在相同的平衡体系中,加入溶液后,点滴板孔中溶液的颜色加深,加入KSCN溶液后点滴板孔中的溶液颜色也加深,说明任一反应物浓度的增加均使平衡向正反应方向移动
【问题】为什么增加任一反应物的浓度都能促使平衡向正反应方向移动
(试从浓度的变化如何影响V正、V逆的速率来解释原因)浓度对平衡影响的v-t图分析1V正V逆′′V速率V正V逆0t时间t1平衡向正反应方向移动浓度对平衡影响的v-t图分析2V正V逆′′V速率V正V逆0t时间V逆V正′′V速