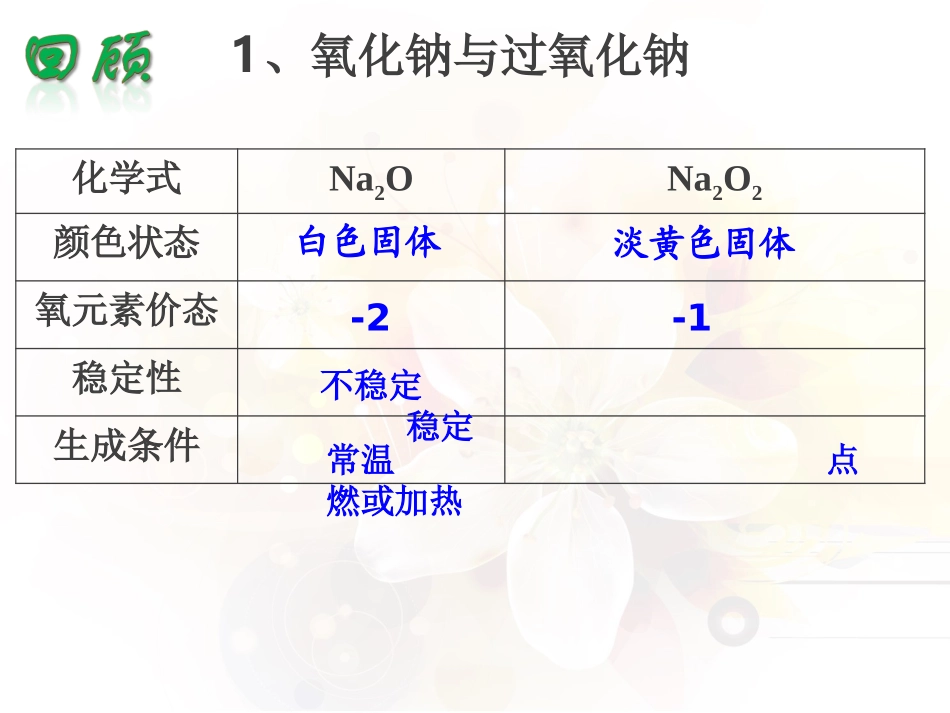
第二节几种重要的金属化合物一、钠的重要化合物生活中钠的化合物1、氧化钠与过氧化钠化学式Na2ONa2O2颜色状态氧元素价态稳定性生成条件白色固体淡黄色固体-1-2不稳定稳定常温点燃或加热与H2O反应与CO2反应与酸反应思考:已知氧化钠是碱性氧化物,你推测它能与哪些物质发生反应
与H2O反应Na2O+H2O=2NaOH类比:生石灰加水生成熟石灰CaO+H2O=Ca(OH)2过氧化钠与水反应(1)带火星的木条复燃(2)试管外壁热(3)滴加酚酞,溶液呈红色(4)振荡,红色褪去有O2生成反应放热有碱生成将水加入盛有Na2O2的试管中,并将带火星的木条放在管口,随后滴入几滴酚酞试液
现象解释Na2O2有漂白性2Na2O2+2H2O=4NaOH+O2↑氧化性:氧化剂>氧化产物用途:Na2O2是强氧化剂,可做漂白剂(氧化性漂白)Na2O2>O2得到2e-,化合价降低,被还原2Na2O2+2H2O=4NaOH+↑失去2e-,化合价升高,被氧化-1-2-20O2练习:用双线桥分析电子转移的方向和数目与CO2反应Na2O+CO2=Na2CO3Na2O2+CO2=失去2e-,化合价升高,被氧化得到2e-,化合价降低,被还原2Na2O2+2CO2=2Na2CO3+O2应用:呼吸面具、潜艇、航空航天中的供氧剂
Na2O+2HCl=2NaCl+H2OCaO+2HCl=CaCl2+H2OCuO+2HCl=CuCl2+H2O与盐酸反应金属氧化物+酸==盐+水思考:对比Na2O、Na2O2分别与水和二氧化碳反应原理的异同点,推测Na2O2与盐酸反应产物,并书写化学反应方程式碱性氧化物2Na2O2+4HCl=4NaCl+2H2O+O2↑化学式Na2ONa2O2颜色状态氧元素价态稳定性生成条件与水反应与CO2反应与盐酸反应类别、特性1、氧化钠与过氧化钠淡黄色固体白色固体-2价-1价常温点燃或加热Na2O+H2O