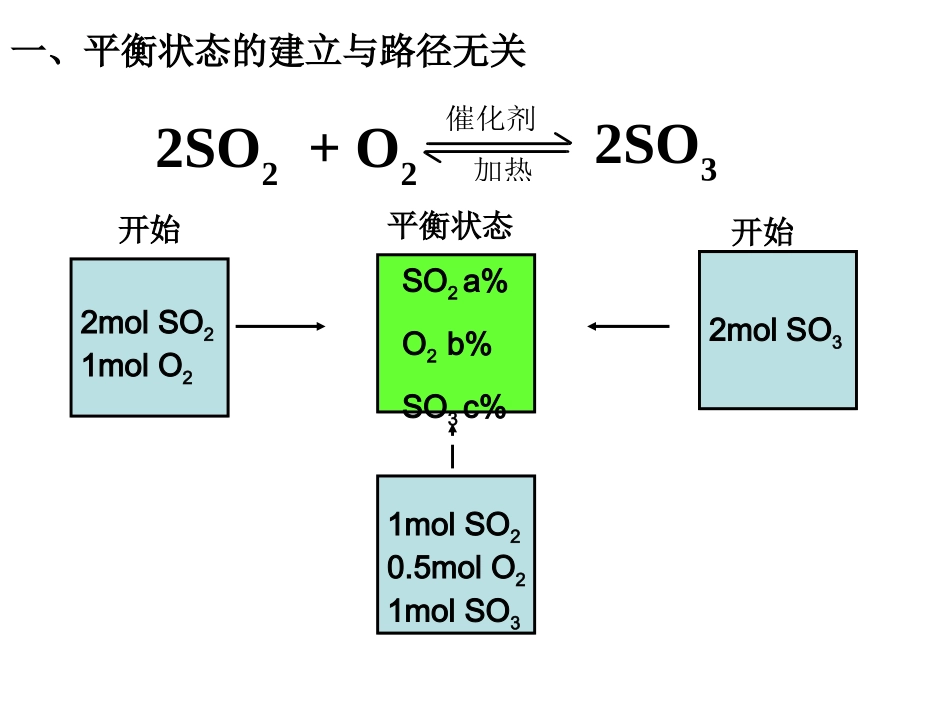
2molSO21molO2开始2molSO3开始SO2a%O2b%SO3c%平衡状态1molSO20
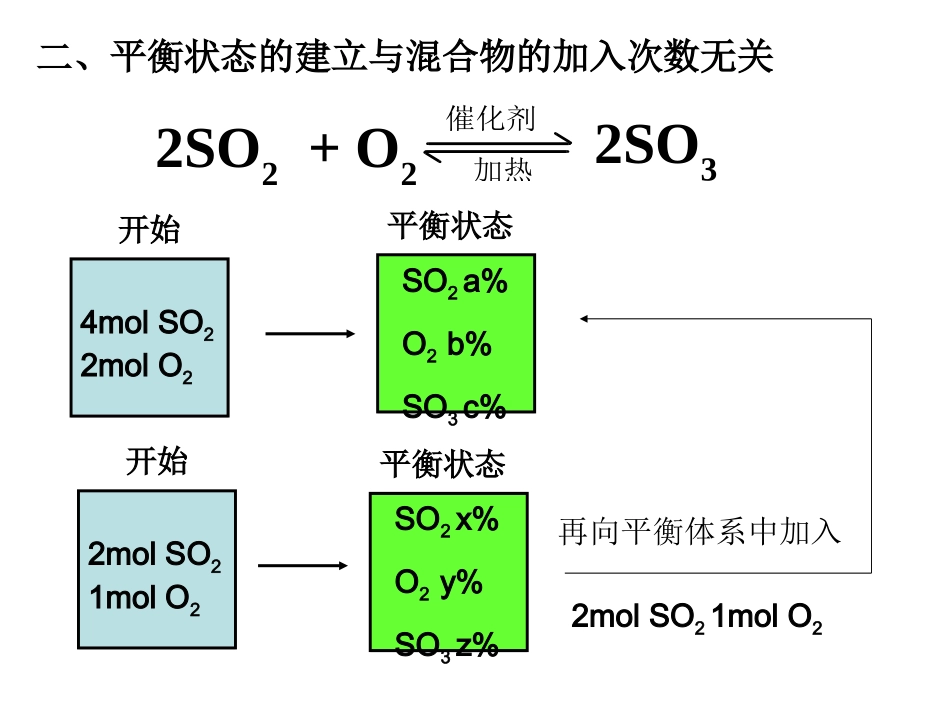
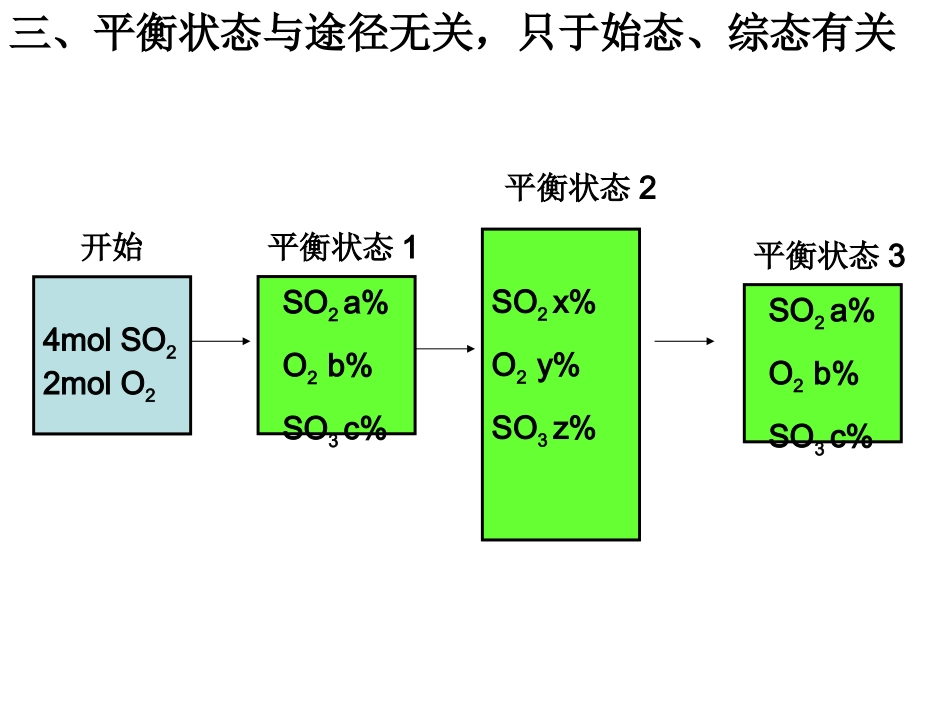
5molO21molSO32SO2+O2催化剂加热2SO3一、平衡状态的建立与路径无关二、平衡状态的建立与混合物的加入次数无关2SO2+O2催化剂加热2SO34molSO22molO2开始SO2a%O2b%SO3c%平衡状态2molSO21molO2开始平衡状态再向平衡体系中加入2molSO21molO2SO2x%O2y%SO3z%三、平衡状态与途径无关,只于始态、综态有关SO2x%O2y%SO3z%平衡状态24molSO22molO2开始SO2a%O2b%SO3c%平衡状态1SO2a%O2b%SO3c%平衡状态3四、平衡混合物的百分含量与物质的量2SO2+O2催化剂加热2SO3平衡状态平衡状态SO2%=a%n(SO2)=bSO2%=
n(SO2)=
n(SO2)=
解题模型建立2SO2+O2催化剂加热2SO3例1:2molSO21molO2开始平衡状态4molSO22molO2开始平衡状态情况一情况二恒温恒容条件下SO2%=an(SO2)=bSO2%=cn(SO2)=d比较a与c、b与d的大小关系298K1L298K1L2SO2+O2催化剂加热2SO3例2:2molSO21molO2开始平衡状态4molSO22molO2开始平衡状态情况一情况二恒温恒压条件下SO2%=an(SO2)=bSO2%=cn(SO2)=d比较a与c、b与d的大小关系298K1L298K2L思考:4molSO22molO2开始平衡状态平衡状态2SO2+O2催化剂加热2SO3等T、V等T、PSO2%=an(SO2)=bSO2%=cn(SO2)=d比较a与c、b与d的大小关系例3:1molH21molBr2开始平衡状态2molH22molBr2开始平衡状态情况一情况二恒温恒容条件下H2%=a