1“氧化还原”专题复习学案——针对学生的障碍点进行突破环节一:标识下列物质核心元素的化合价Cr2O3Cr2O72-CrO42-S2O32-FeO42-Fe3O4MnO42-MnO4-C2O42-NH3CN-OCN-SOCl2N2H4CH4CH3OHCH3CH2OHCH3CHOCH3COOH1-1.我国工业废水排放是有严格规定的
下列说法不正确的是A.废水中的Hg2+、Cd2+、Pb2+是重金属离子B.对于pH>9的废水可用中和法处理C.将CrO42-转化为Cr2O72-是用氧化还原的方法D.在含有Hg2+的废水中加入Na2S,可使Hg2+转变成沉淀而除去1-2.处理含氰(CN-)废水涉及以下反应,其中无毒的OCN-中碳元素为+4价
CN-+OH-+Cl2→OCN-+Cl-+H2O(未配平)···········反应I2OCN-+4OH-+3Cl2=2CO2+N2+6Cl-+2H2O···········反应II下列说法正确的是A.反应I中碳元素被还原B.反应II中CO2为氧化产物C.处理过程中,每产生1molN2,消耗3molCl2D.反应I中CN-与Cl2按物质的量之比1︰1进行反应1-3.含氮、磷污水过量排放引起的水体富营养化是当前备受关注的环境问题
氮的化合物在水中被细菌分解,当氧气不充足时,在反硝化细菌的作用下,细菌利用有机物(又称碳源,如甲醇)作为电子供体,将硝态氮的化合物(含NO3-)连续还原最终生成N2,发生反硝化作用,完成下述反应的方程式:+5CH3OH↑+CO32-+4HCO3-+环节二:氧化还原反应“有升必有降”书写氧还方程式的基本构成,并用双线桥法表示得失电子和化合价变化
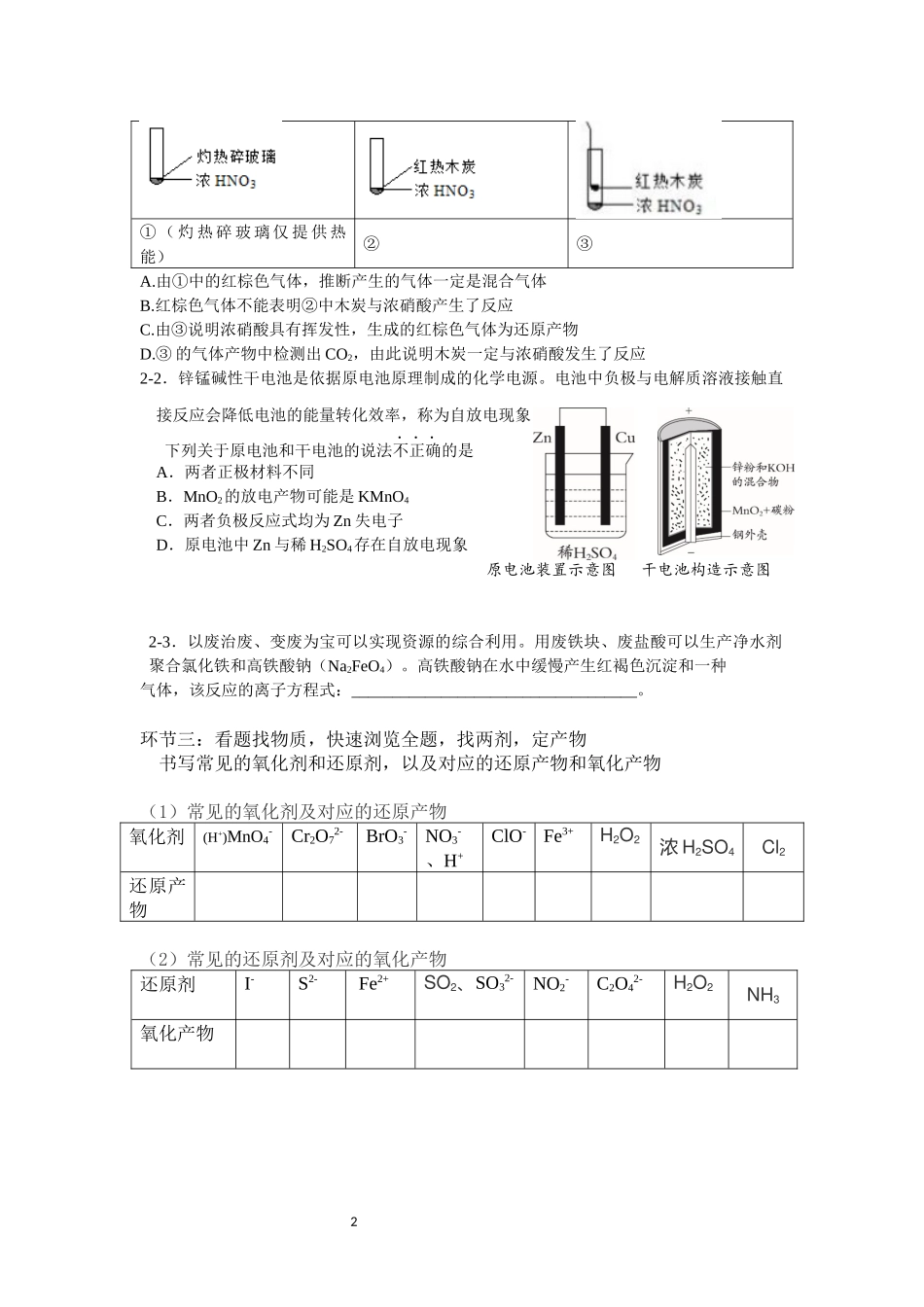
下述实验中均有红棕色气体产生,对比分析所的结论不正确的是氧化剂+还原剂==还原产物+氧化产物2①(灼热碎玻璃仅提供热能)②③A
由①中的红棕色气体,推断产生的气体一定是混合气