定量实验专题复习------混合物中某物质质量分数的测定一、教学目标1
能根据实验装置和实验步骤分析实验的原理,能根据实验原理和物质的性质明确实验装置和实验操作在实验中起的作用
能通过数据的分析总结出一般规律和结论
学会对实验方案进行评价和改进,学会进行误差分析
二、教学重点、难点重点:实验原理与数据分析难点:误差分析三、教学过程可能用到的相对原子质量:C-12O-16Na-23Ba-137S-32【典型例题】1
某研究性学习小组为测定纯碱样品(含NaCl杂质)中碳酸钠质量分数设计了如下实验方案
实验步骤如下:①用托盘天平称取ag的纯碱样品放入烧杯中加水充分溶解;②向上述所得溶液中加入过量的BaCl2溶液,充分反应后过滤、洗涤、干燥、称量沉淀的质量为mg;回答下列问题:(1)步骤②中发生的化学反应方程式为___________________________________________
(2)证明反应后BaCl2过量的方法是____________________________________________;(3)样品中碳酸钠的质量分数为________________________________
(用含字母的式子表示)2
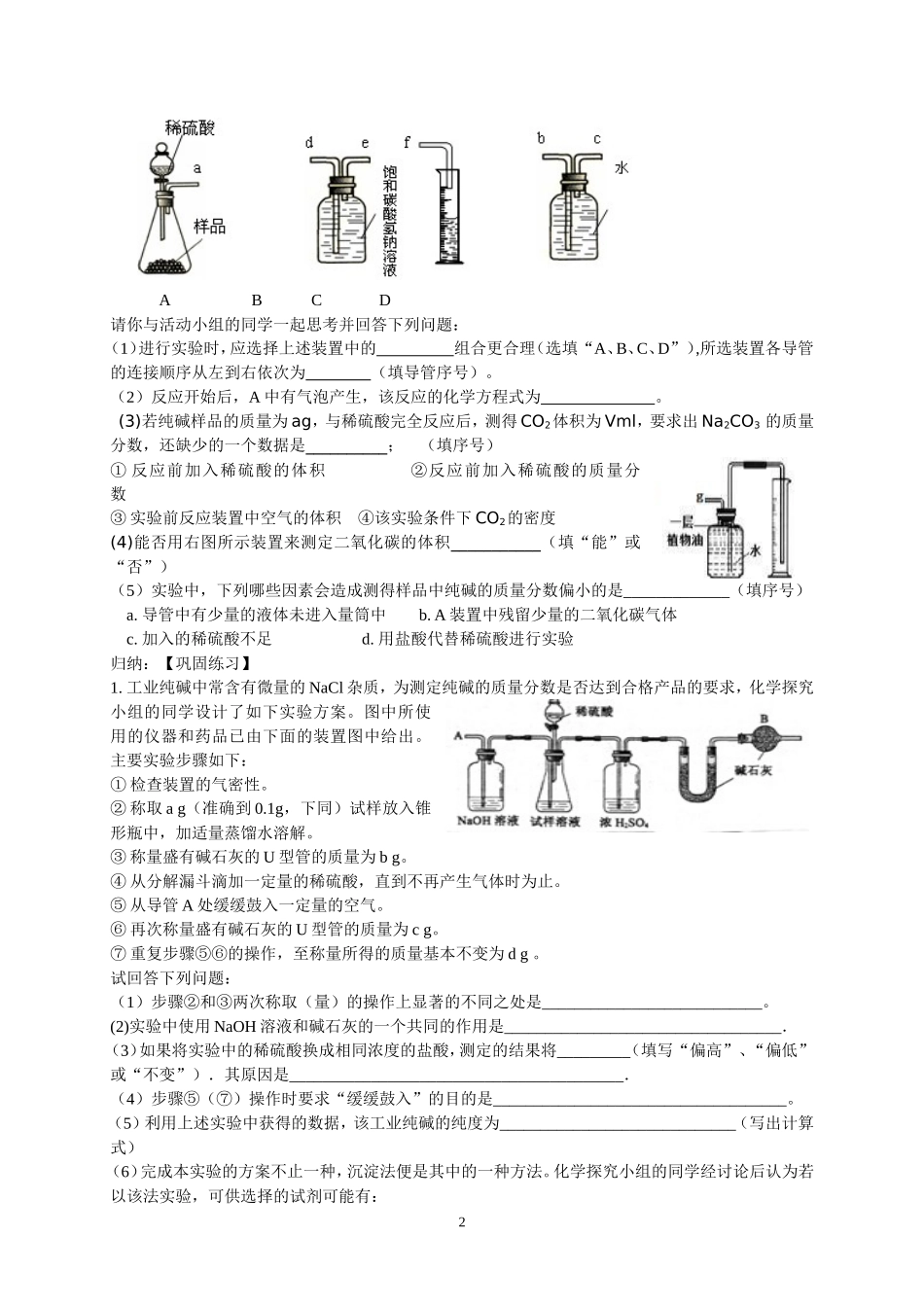
某纯碱样品中含有少量氯化钠杂质,现用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去)
实验步骤如下:①检查装置气密性;②准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量为83
4g;③准确称得6g纯碱样品放入容器B中;④先连接好装置A、B、C,打开弹簧夹,缓缓鼓入空气数分钟后关闭弹簧夹,再接上装置D和E;⑤打开分液漏斗活塞a,缓缓滴入稀硫酸,至不再产生气泡为止;⑥再次打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85
试回答:(1)步骤④鼓入空气的目的是____