32、化学实验知识的综合应用1.以六水合氯化镁(MgCl2·6H2O)为原料制备无水氯化镁
已知MgCl2·6H2O晶体在空气中加热时,释放出部分结晶水,同时生成Mg(OH)Cl或MgO;在干燥HCl气流中加热,能制得无水MgCl2
可选用药品:MgCl2·6H2O晶体、NaCl(s)、KClO3(s)、MnO2、浓H2SO4、浓盐酸、稀NaOH溶液
仪器如图所示(装置可重复使用)
回答下列问题:(1)组装氯化氢气体发生器,应选用的仪器(用编号A、B等填入)是______,有关的化学方程式是______________
(2)按气流方向,其余装置的连接顺序(用数字①、②等填入)是:()→()()→()()→()()
(3)各装置中应放的药品:A.______,B.______,C.______,D.______,E.______
(4)B装置的作用是_________,B中能观察到的现象是__________
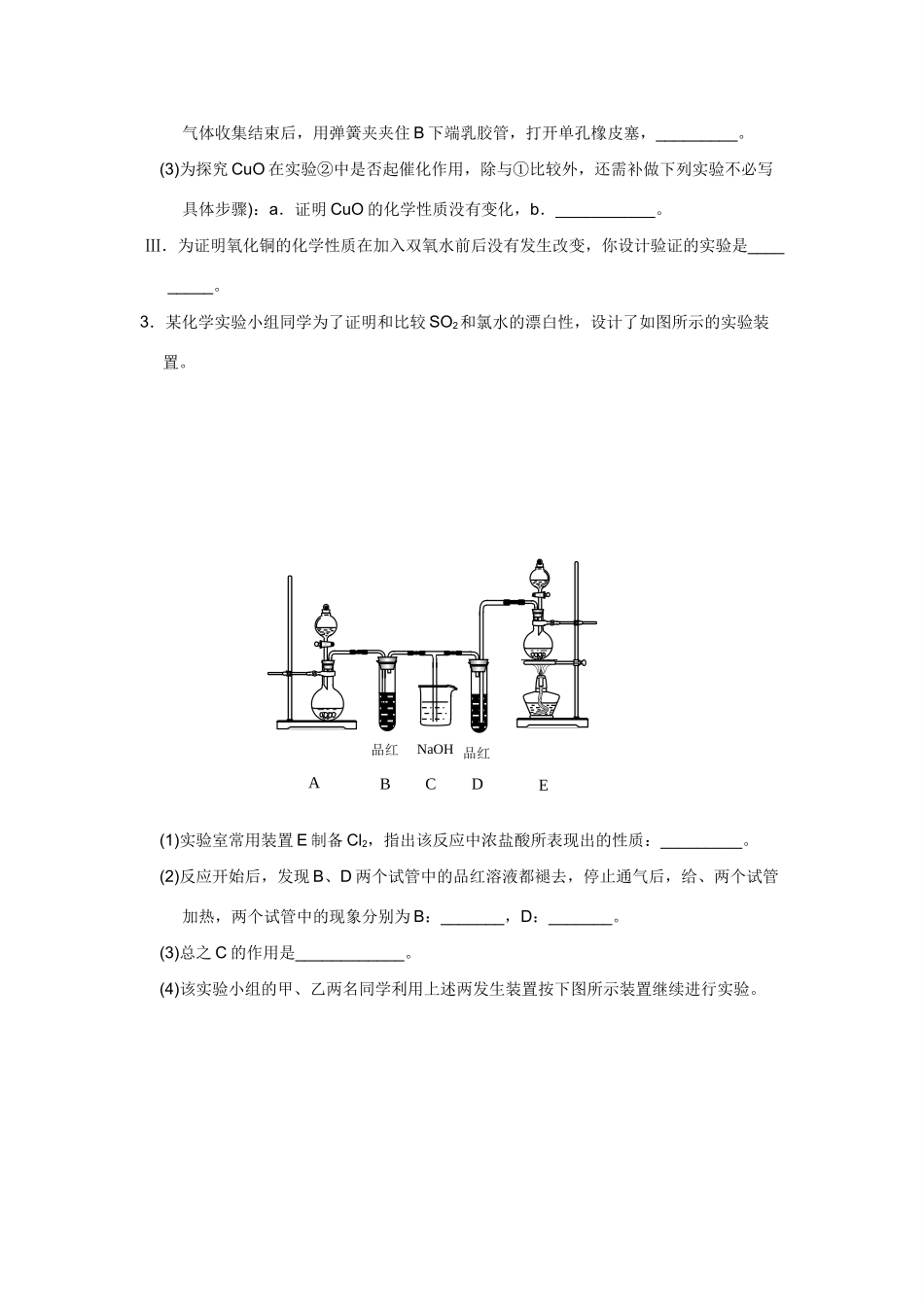
2.某实验小组欲用10g胆矾制取氧化铜并证明氧化铜能加快氯酸钾的分解
①②③④⑤⑥⑦ABCEFABCⅠ.请你完成他们制取氧化铜的实验步骤
(1)称取10g胆矾,将其放入小烧杯中,再_______
(2)向步骤(1)中的烧杯内滴加______溶液,直至产生大量的沉淀
(3)检验沉淀是否完全,操作方法是__________
(4)将步骤(2)所得混合物加热至测定全部变为_____色
(5)再将步骤(4)所得混合物_____、洗涤、______后研细;验证是否洗净沉淀中的硫酸根离子的方法是_____________
Ⅱ.请用图中所示实验装置证明氧化铜能加快约7%的双氧水的分解并与二氧化锰的催化效果进行比较(即比较反应速率)
用图示装置测量产生气体的体积,其他可能影响实验的因素均已忽略,相关数据如下:(1)从实验原理来看,实验中的“待测数据”可以指_______、也可以指__