专项突破练(八)加试第31题1.(2016·台州9月选考质量评估)CaO2(过氧化钙)在医用防腐、消毒等方面应用广泛
它难溶于水、乙醇等溶剂,易溶于酸,温度过高易分解释放出氧气
实验室以大理石(含少量SiO2等杂质)为原料制备过氧化钙及含量测定如下:(一)过氧化钙的制备流程大理石―――――――――――→滤液――――――――――→――→滤渣――→――→产品已知:CaCl2+2NH3·H2O+H2O2+6H2O===CaO2·8H2O↓+2NH4Cl(1)步骤①的具体操作为逐滴加入适量稀盐酸,将溶液煮沸,趁热过滤
将溶液煮沸的作用是_____________
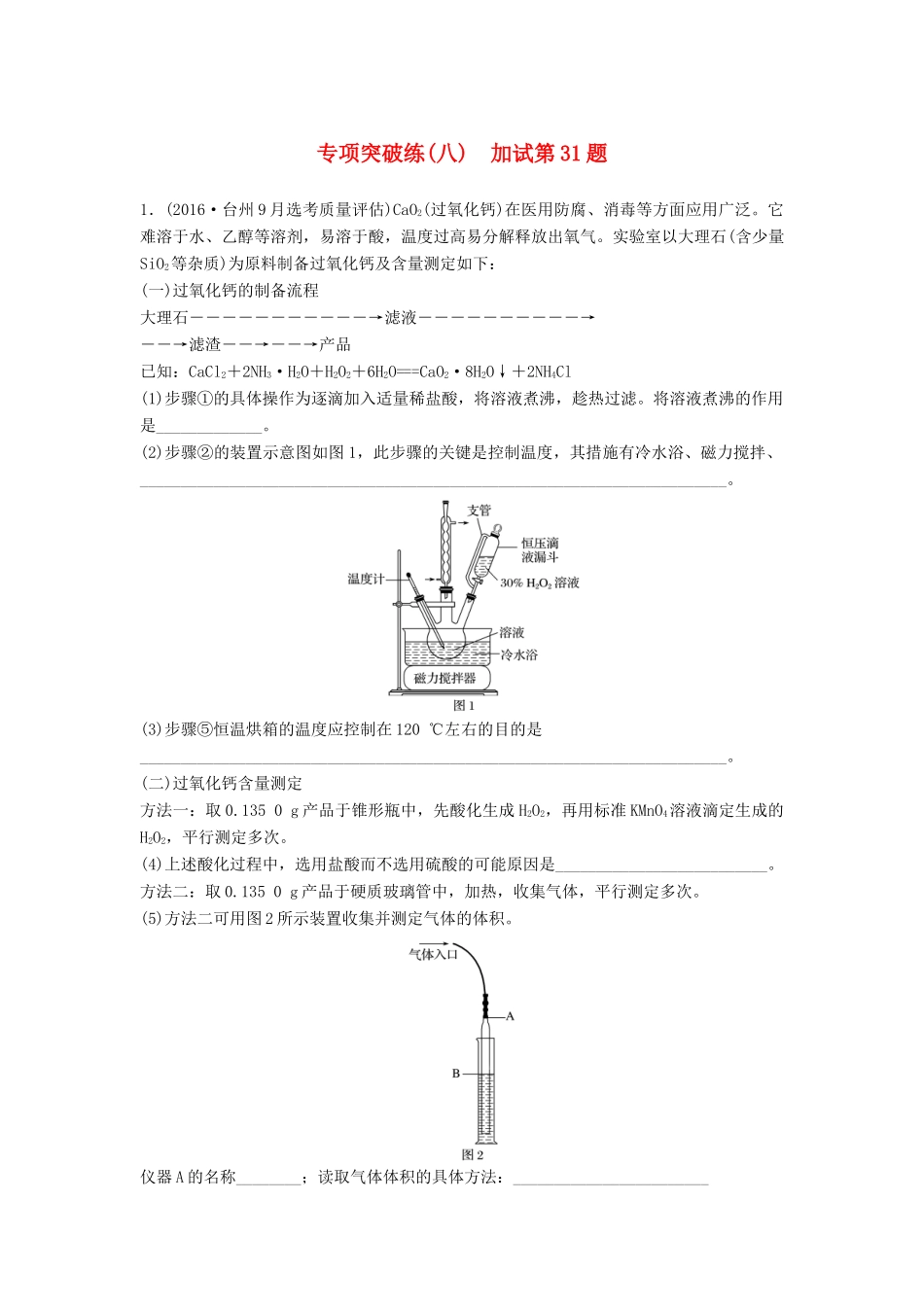
(2)步骤②的装置示意图如图1,此步骤的关键是控制温度,其措施有冷水浴、磁力搅拌、________________________________________________________________________
(3)步骤⑤恒温烘箱的温度应控制在120℃左右的目的是________________________________________________________________________
(二)过氧化钙含量测定方法一:取0
1350g产品于锥形瓶中,先酸化生成H2O2,再用标准KMnO4溶液滴定生成的H2O2,平行测定多次
(4)上述酸化过程中,选用盐酸而不选用硫酸的可能原因是__________________________
方法二:取0
1350g产品于硬质玻璃管中,加热,收集气体,平行测定多次
(5)方法二可用图2所示装置收集并测定气体的体积
仪器A的名称________;读取气体体积的具体方法:_____________________________________________________________________________________________