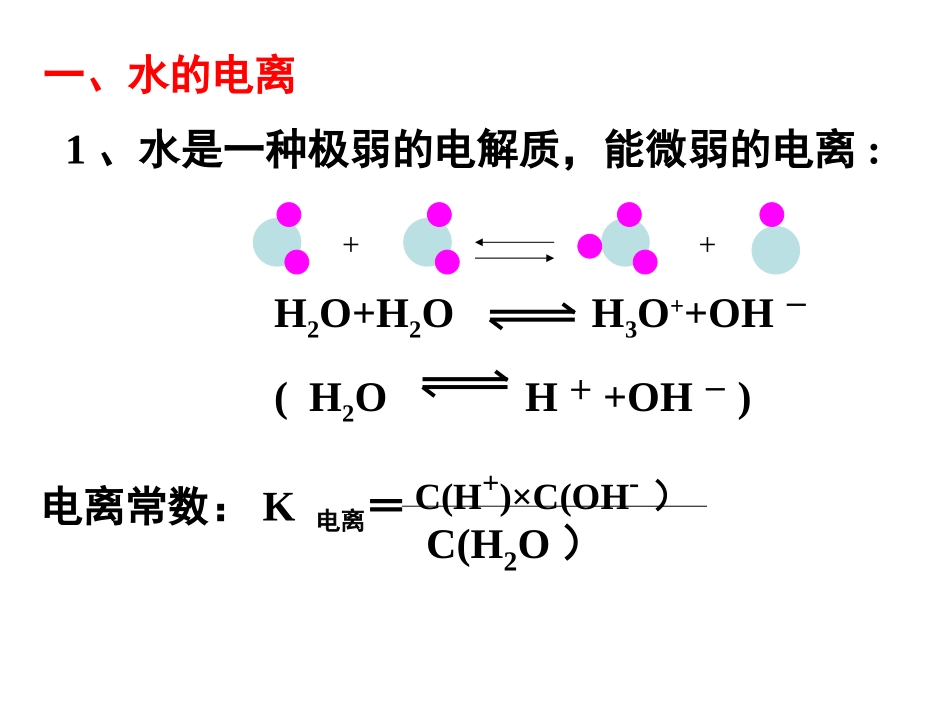
专题3溶液中的离子反应常见的弱电解质闽侯四中高二化学备课组叶贵旺一、水的电离1、水是一种极弱的电解质,能微弱的电离:++H2O+H2OH3O++OH-(H2OH++OH-)电离常数:K电离=C(H+)×C(OH-)C(H2O)【思考与交流】你能算出纯水或稀溶液中的c(H2O)吗
纯水或稀溶液的密度为1g/cm3
【思考与交流】解:取1L水或稀溶液c(H2O)=n(H2O)/V(液)=m(H2O)/[M(H2O)V(液)]=[V(液)ρ(H2O)]/[M(H2O)V(液)]=1000/18=55
56mol/L在一定温度时:C(H+)×C(OH-)=Kw,叫水的离子积25℃时,Kw=1×10-141、水的离子积水的浓度为常数,K电离也是常数所以K电离×C(H2O)=C(H+)×C(OH-)为一个新的常数
提问:常数是否就不变呢
根据前面所学知识,水的离子积会受什么外界条件影响
C(H+)=C(OH-)=1×10-7mol/LKW=【小结】(1)Kw取决于温度,不仅适用于纯水,还适用于其他溶液
(2)在水溶液中,Kw中的C(OH-)、C(H+)指溶液中总的离子浓度
(3)常温下,任何稀的水溶液中,Kw=C(H+)×C(OH-)=1×10-14(4)不论是在中性溶液还是在酸碱性溶液,水电离出的C(H+)=C(OH-)(5)根据Kw=C(H+)×C(OH-)在特定温度下为定值,C(H+)和C(OH-)可以互求
1、25℃时,向纯水中加入少量氯化氢气体,仍能保持不变的是()A.c(H+)B.c(OH-)C.KwD.c(H+)/c(OH-)2、纯水在10℃和50℃的H+浓度,前者与后者的关系是()A、前者大B、后者大C、相等D、不能确定3、某温度下纯水中C(H+)=2×10-7mol/L,则此时溶液中的C(OH-)=___________
若温度不变,滴入稀盐酸使C(H+)=5×10-