专题14原电池化学电源考点一原电池的工作原理[考试标准]知识条目必考要求加试要求1
原电池的概念aa2
铜锌原电池的原理及电极反应式bb3
原电池的构成条件ab4
原电池的构造与工作原理,盐桥的作用b5
判断与设计简单的原电池c6
原电池的电极反应式及电池反应方程式b7
原电池的正、负极和电子流向的判断c1.概念和反应本质原电池是把化学能转化为电能的装置,其反应本质是氧化还原反应
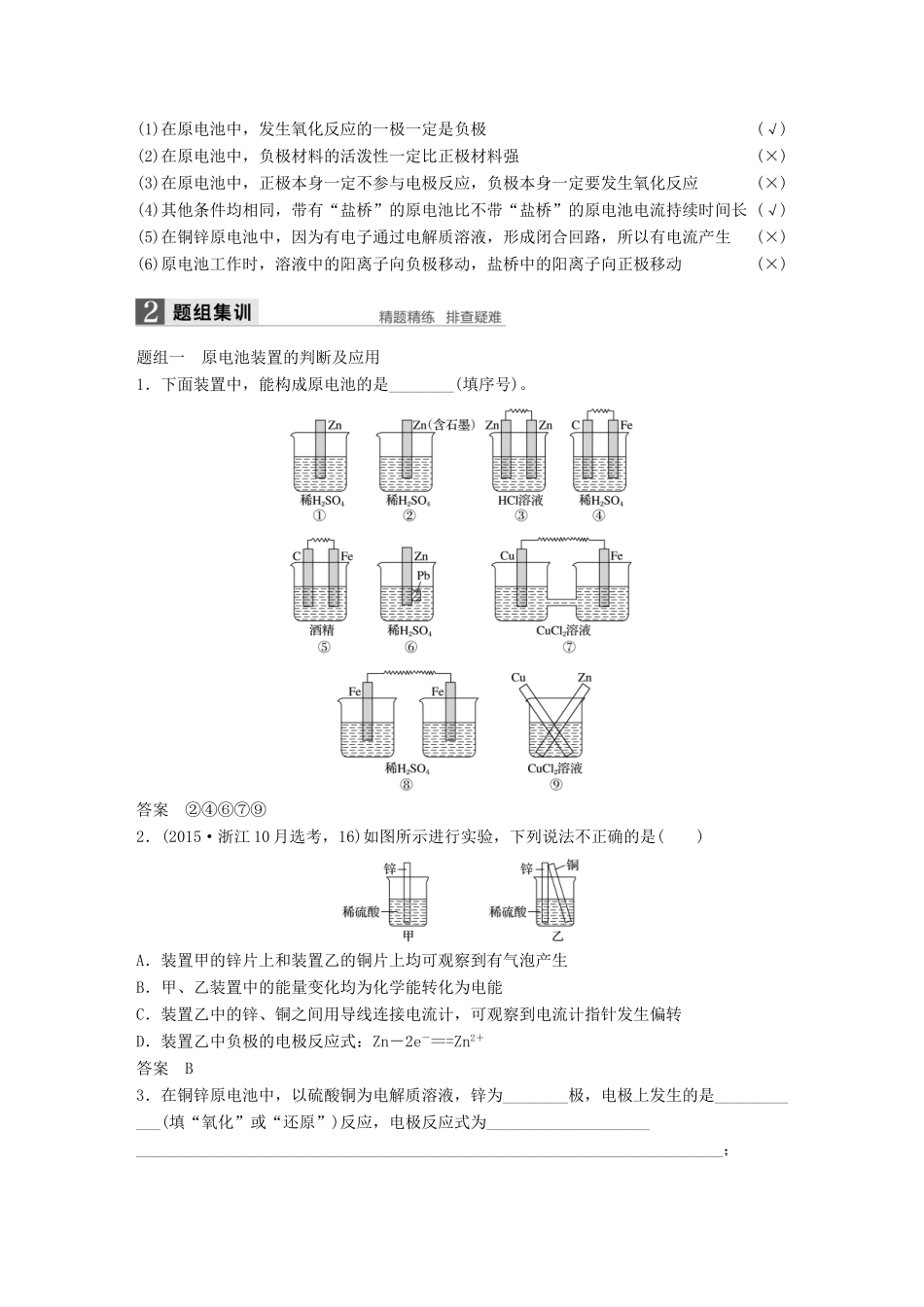
2.工作原理(1)反应原理电极名称负极正极电极材料锌片铜片电极反应Zn-2e-===Zn2+Cu2++2e-===Cu反应类型氧化反应还原反应电子流向由Zn片沿导线流向Cu片(2)原理归纳3.原电池的构成条件(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶液反应)
(2)二看两电极:一般是活泼性不同的两电极
(3)三看是否形成闭合回路,形成闭合回路需三个条件:①电解质溶液;②两电极直接或间接接触;③两电极插入电解质溶液中
4.盐桥原电池(加试)(1)构造(2)盐桥的组成和作用①盐桥中装有饱和的KCl、KNO3等溶液和琼脂制成的胶冻
②盐桥的作用a.连接内电路,形成闭合回路;b.平衡电荷,使原电池不断产生电流
③盐桥含饱和KCl溶液,K+移向正极,Cl-移向负极
(3)单池原电池和盐桥原电池的对比图1和图2两装置的相同点:正负极、电极反应、总反应、反应现象
负极:Zn-2e-===Zn2+正极:Cu2++2e-===Cu总反应:Zn+Cu2+===Cu+Zn2+不同点:图1中Zn在CuSO4溶液中直接接触Cu2+,会有一部分Zn与Cu2+直接反应,该装置中既有化学能和电能的转化,又有一部分化学能转化成了热能,装置的温度会升高
图2中Zn和CuSO4溶液分别在两个池子中,Zn与Cu2+不直接接触,不存在Zn与Cu2+直接反应的过程,所以仅是化学能转化成了电能,电流稳