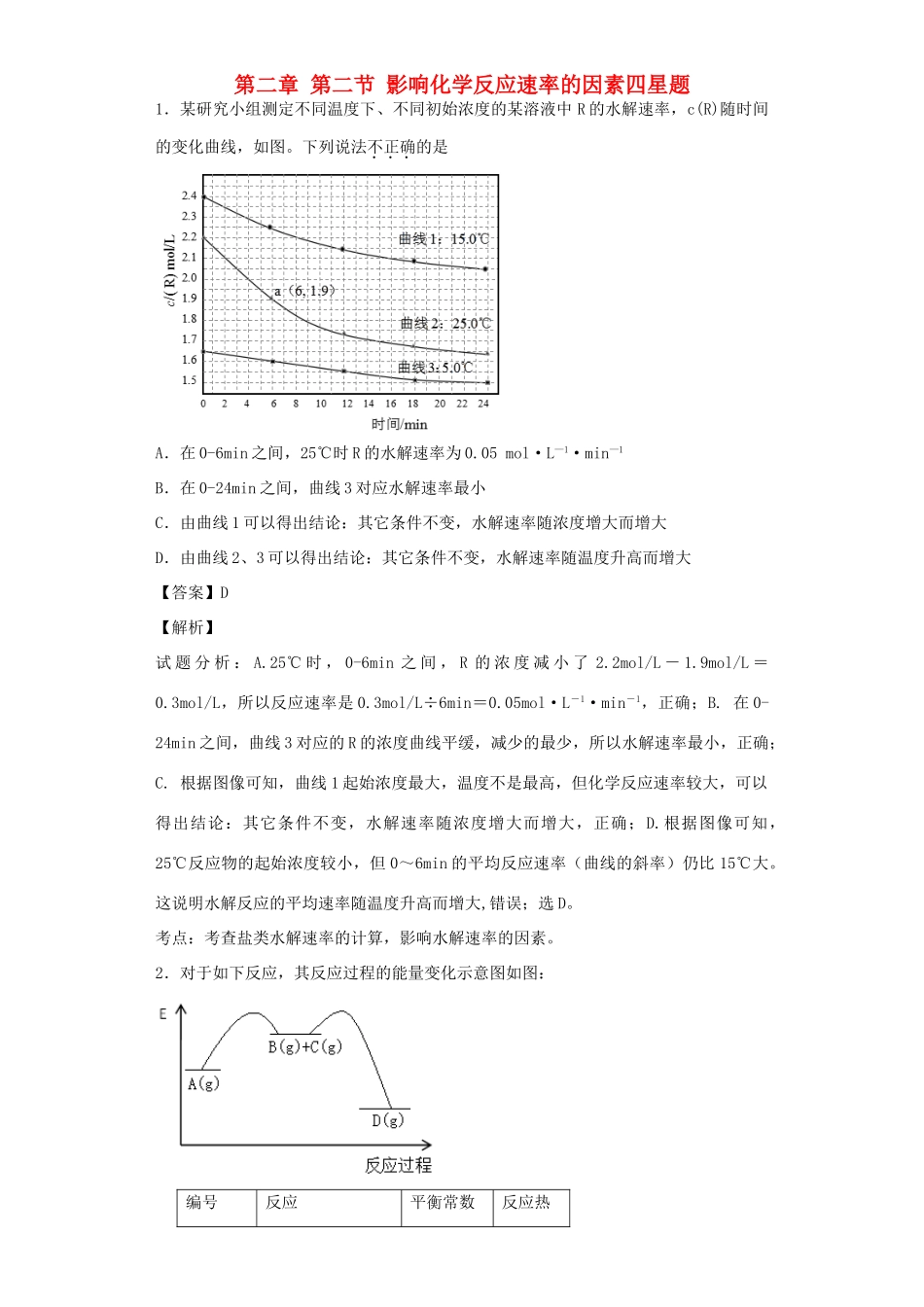
第二章第二节影响化学反应速率的因素四星题1.某研究小组测定不同温度下、不同初始浓度的某溶液中R的水解速率,c(R)随时间的变化曲线,如图
下列说法不正确的是A.在0-6min之间,25℃时R的水解速率为0
05mol·L—1·min—1B.在0-24min之间,曲线3对应水解速率最小C.由曲线1可以得出结论:其它条件不变,水解速率随浓度增大而增大D.由曲线2、3可以得出结论:其它条件不变,水解速率随温度升高而增大【答案】D【解析】试题分析:A
25℃时,0-6min之间,R的浓度减小了2
2mol/L-1
9mol/L=0
3mol/L,所以反应速率是0
3mol/L÷6min=0
05mol·L-1·min-1,正确;B
在0-24min之间,曲线3对应的R的浓度曲线平缓,减少的最少,所以水解速率最小,正确;C
根据图像可知,曲线1起始浓度最大,温度不是最高,但化学反应速率较大,可以得出结论:其它条件不变,水解速率随浓度增大而增大,正确;D
根据图像可知,25℃反应物的起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大
这说明水解反应的平均速率随温度升高而增大,错误;选D
考点:考查盐类水解速率的计算,影响水解速率的因素
2.对于如下反应,其反应过程的能量变化示意图如图:编号反应平衡常数反应热反应①A(g)=B(g)+C(g)K1△H1反应②B(g)+C(g)=D(g)K2△H2反应③A(g)=D(g)K3△H3下列说法正确的是A.K3=K1+K2B.△H3=△H1+△H2C.加催化剂,反应①的反应热降低,反应速率加快D.则增大压强,K1减小,K2增大,K3不变【答案】B【解析】试题分析:由反应可知、,故K3=K1×K2,故A项错误;由盖斯定律可知△H3=△H1+△H2,故B项正确;催化剂只能降低反应活化能,是活化分子百分率增多,反应速率加快,但不会影响