第三节电解池——电解原理及应用陇西二中王平2017
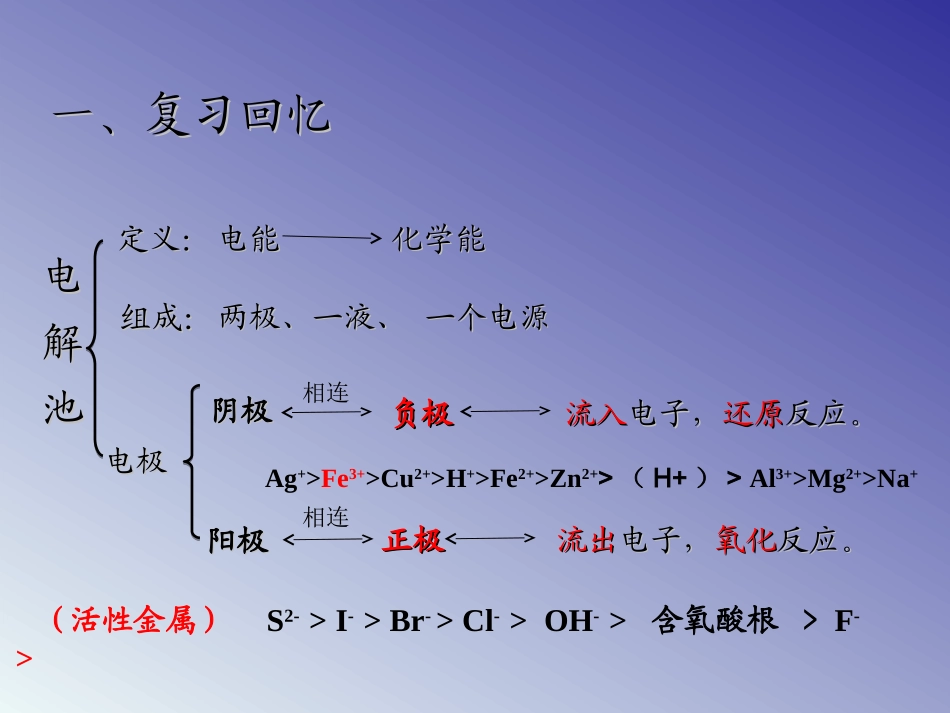
09定义:定义:电能化学能电能化学能组成:组成:两极、两极、一液、一液、一个电源一个电源电极电极阳极阳极正极正极流出流出电子,电子,氧化氧化反应
阴极阴极负极负极流入流入电子,电子,还原还原反应
电解池电解池一、一、复习回忆复习回忆相连相连S2->I->Br->Cl->OH->含氧酸根>F-Ag+>Fe3+>Cu2+>H+>Fe2+>Zn2+>(H+)>Al3+>Mg2+>Na+(活性金属)>11、电极产物的判断(惰性电极)、电极产物的判断(惰性电极)NaClNa+Cl-H+OH-阴极产物及电极方程式阳极产物及电极方程式2Cl--2e-=Cl2↑2H++2e-=H2↑Na+OH-2NaCl+2H2O2NaOH+Cl2↑+H2↑电解练习:用惰性电极电解下列物质的溶液练习:用惰性电极电解下列物质的溶液Na2SO4Na+SO42-H+OH-阴极产物及电极方程式阳极产物及电极方程式4OH--4e-=O2↑+2H2O4H++4e-=2H2↑H+OH-2H2OO2↑+2H2↑电解饱和NaCl溶液石墨石墨阳极:阴极:总反应:2NaCl+2H2O2NaOH+Cl2↑+H2↑电解2Cl--2e-=Cl2↑2H++2e-=H2↑22、、电解原理的应用电解原理的应用————氯碱工业用惰性电极电解NaCl溶液(1)Cl2接触NaOH溶液会反应,反应方程式:
Cl2+2NaOH=NaCl+NaClO+H2O(2)生成物H2和Cl2混合有什么危险
混合遇火或强光能反应(3)如何不让生成物H2和Cl2混合使用离子交换膜将池分开饱和NaCl溶液石墨石墨交流电解饱和食盐水制烧碱、氯气和氢气交流总结+-精制饱和食盐水水(含少量NaOH)Cl2H2NaOH溶液淡盐水Na+阳极:2Cl--2e-=Cl2↑阴极:2H++2e-=H2↑总反应:2N