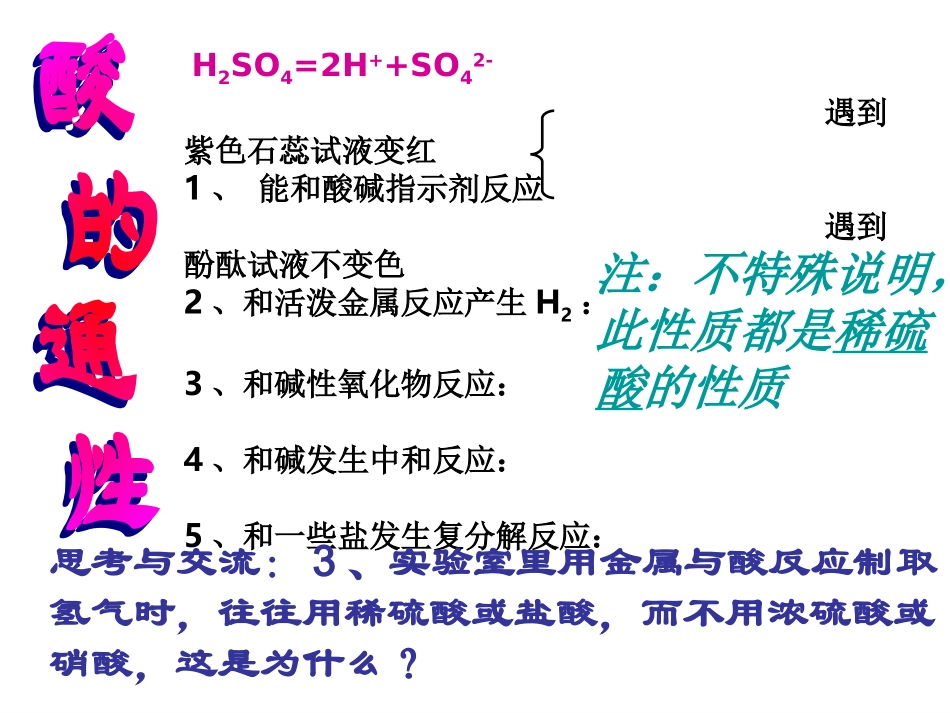
第四节氨硝酸硫酸(第三课时)硫酸和硝酸的氧化性H2SO4=2H++SO42-遇到紫色石蕊试液变红1、能和酸碱指示剂反应遇到酚酞试液不变色2、和活泼金属反应产生H2:3、和碱性氧化物反应:4、和碱发生中和反应:5、和一些盐发生复分解反应:注:不特殊说明,此性质都是稀硫酸的性质思考与交流:3、实验室里用金属与酸反应制取氢气时,往往用稀硫酸或盐酸,而不用浓硫酸或硝酸,这是为什么
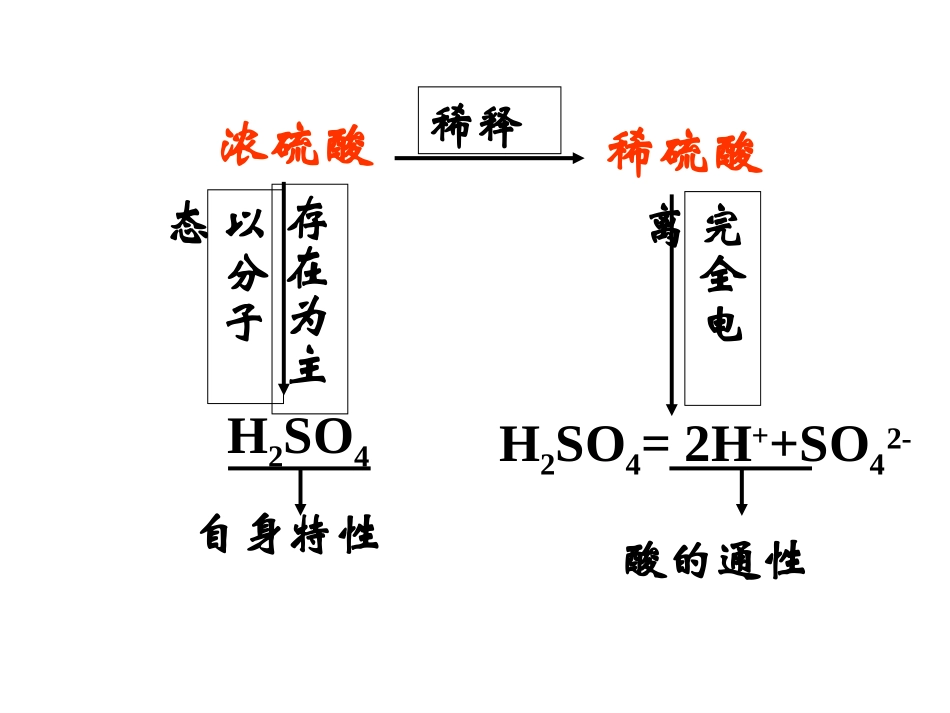
浓硫酸稀硫酸H2SO4H2SO4=2H++SO42-酸的通性稀释完全电离自身特性以分子态存在为主二、浓硫酸的性质:1、物理性质(1)纯净的硫酸是无色油状粘稠的液体(2)质量分数:98
3%;密度:1
84g/cm3(4)沸点:338°C难挥发性(3)易溶于水,并放出大量的热怎样稀释
物质的量浓度为18
4mol/L思考
浓硫酸敞口放置于空气中质量有何变化
浓硫酸本身难挥发,溶质质量不变,但因吸收空气中游离的水溶液质量会增重
若是浓盐酸呢
现有体积相同的浓硫酸和浓盐酸,分别放在等质量的两个试剂瓶中,不用化学方法怎样识别
提起试剂瓶,重者是浓硫酸;振动试剂瓶,液体呈油状的是浓硫酸;打开试剂瓶,瓶口不生白雾者是浓硫酸;打开试剂瓶,无刺激性气味的是浓硫酸
2、浓硫酸的特性——吸水性[探究]a、实验:胆矾晶体中加入少量浓硫酸b、CO2、Cl2中混有水蒸气常用浓硫酸干燥
c、浓硫酸敞口放置如何
[观察与分析]a、胆矾晶体变白
(失去结晶水)c、浓硫酸敞口放置会变稀[结论]浓硫酸具有吸水性(H2SO4+nH2O==H2SO4·nH2O)[探究实验]向盛有蔗糖的烧杯中加入几滴水,搅拌均匀,再加入浓硫酸,迅速搅拌
a、杯壁变热C12H22O11蔗糖浓硫酸12C+11H2O(浓硫酸遇水放热)(气体放出)(产生SO2气体)2、浓硫酸的特性——脱水性b、蔗糖逐渐变黑c、杯内黑色固体体积膨胀d、闻到刺激性气味[结论]体现了浓硫酸的