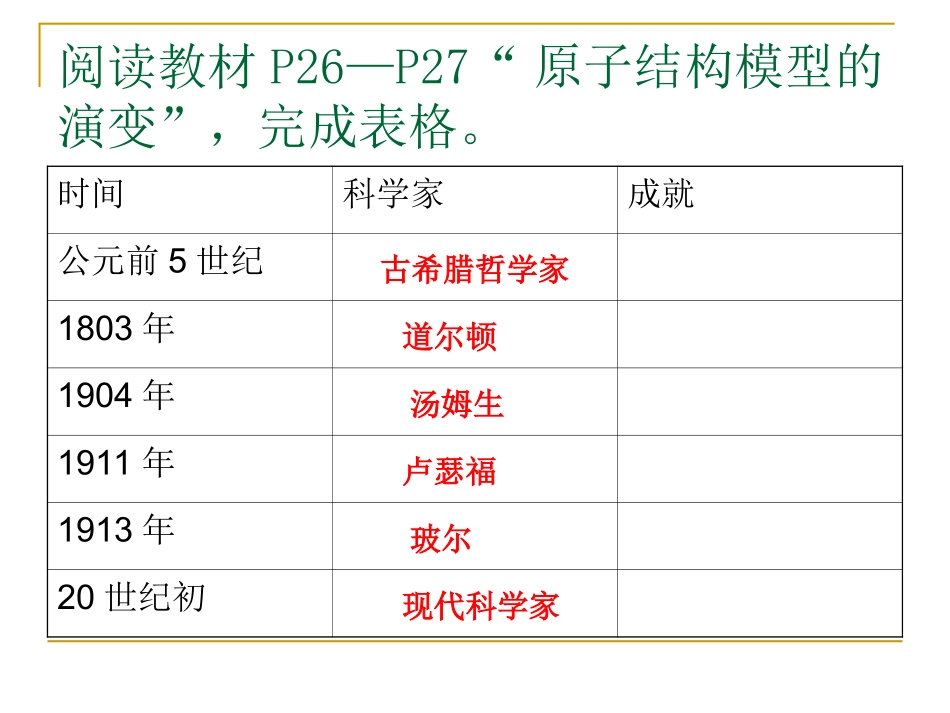
第三单元人类对原子结构的认识原子结构模型的演变2014-10阅读教材P26—P27“原子结构模型的演变”,完成表格。时间科学家成就公元前5世纪1803年1904年1911年1913年20世纪初道尔顿古希腊哲学家汤姆生卢瑟福玻尔现代科学家原子核外电子的排布的规律规律:⑴、对于多电子原子,原子核外电子是分层排布的,原子的核外电子数越多,占据的电子层越多。⑵、原子结构示意图。思考稀有气体的性质与其原子核外电子的排布有什么联系?元素化合价与原子核外电子数的关系1、活泼金属钠、镁、铝可与活泼非金属氟、氧形成氟化物NaF、MgF2、AlF3和氧化物Na2O、MgO、Al2O3。钠、镁、铝、氟、氧的原子核外电子分层排布的示意图如下图所示。请说明下述过程中原子核外最外层电子的变化情况。Na+F→NaFMg+2F→MgF22Na+O→Na2O2Al+3O→Al2O32、有A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18;A原子核内仅有1个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍;E元素的最外层电子数是其电子层数的三分之一。(1)试推断它们各是什么元素,写出它们的元素符号:A______、B______、C.______、D______、E。(2)写出A分别与B、C、D所形成化合物的化学式:。(3)A、C、D形成的化合物与A、D、E形成的化合物各属于那类物质?写出它们相互反应的化学方程式。作业同步练习P20:1~8预习