教学目标1、掌握一种溶液的表示方法----溶质的质量分数,能进行溶质质量分数的简单计算
2、初步学会配制一定溶质质量分数的溶液
药品:水10mL硫酸铜仪器:试管滴管颜色:淡蓝蓝色深蓝实验9-50
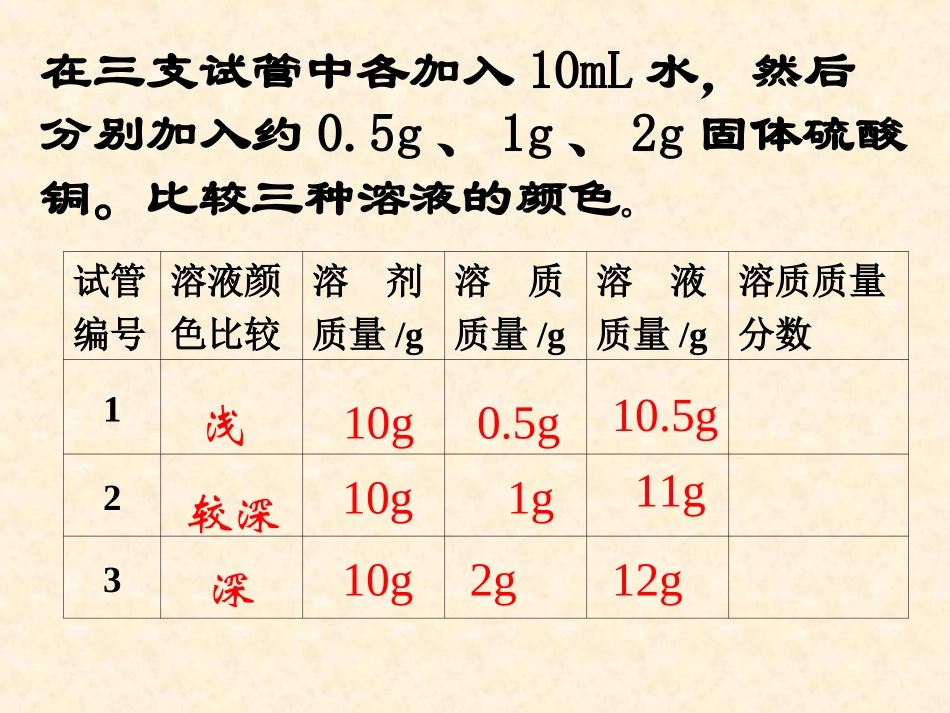
0g2g在三支试管中各加入10mL水,然后分别加入约0
5g、1g、2g固体硫酸铜
比较三种溶液的颜色
试管编号溶液颜色比较溶剂质量/g溶质质量/g溶液质量/g溶质质量分数123浅较深深10g10g10g0
5g1g2g10
5g11g12g•在两杯相同体积的水中分别加入一勺糖、两勺糖,你知道哪个杯子里的水甜吗
•那要在盛有8克蔗糖的烧杯中加入40毫升的水,在盛有10克蔗糖的烧杯中加入50毫升的水,哪个烧杯中水更甜呢
•那就需要我们通过计算来证明,准确知道一定量溶液里含有多少溶质
•你知道需要的公式是什么吗
一、溶质的质量分数1、概念:溶质质量与溶液质量之比
2、计算公式:溶质质量溶液质量溶质的质量分数100%溶质质量溶质质量+溶剂质量100%在三支试管中各加入10mL水,然后分别加入约0
5g、1g、2g固体硫酸铜
比较三种溶液的颜色
试管编号溶液颜色比较溶剂质量/g溶质质量/g溶液质量/g溶质质量分数123浅较深深10g10g10g0
5g1g2g10
5g11g12g4
7%想一想:上述实验配制的溶液中氯化钠的质量分数是多少
[实验9-6]溶质质量溶剂质量溶液中溶质质量分数10g20g90g80g10%20%例1、在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种
现要配制150Kg这种溶液,需要氯化钠和水的质量各是多少
解:溶质质量溶液质量溶质的质量分数100%溶质质量溶液质量溶质的质量分数150Kg16%24Kg溶剂质量溶液质量溶质质量150Kg24Kg126Kg练习配制500mL质量分数为10%的氢氧化钠溶液(密度为1
1g/cm3),需