第二节分子的立体构型C的价电子中只有两个未成对电子,为什么CH4分子中C形成四个共价键
3个相互垂直的2p和一个球形的2s与氢原子4个1s原子轨道重叠不可能得到正四面体构型的甲烷疑问
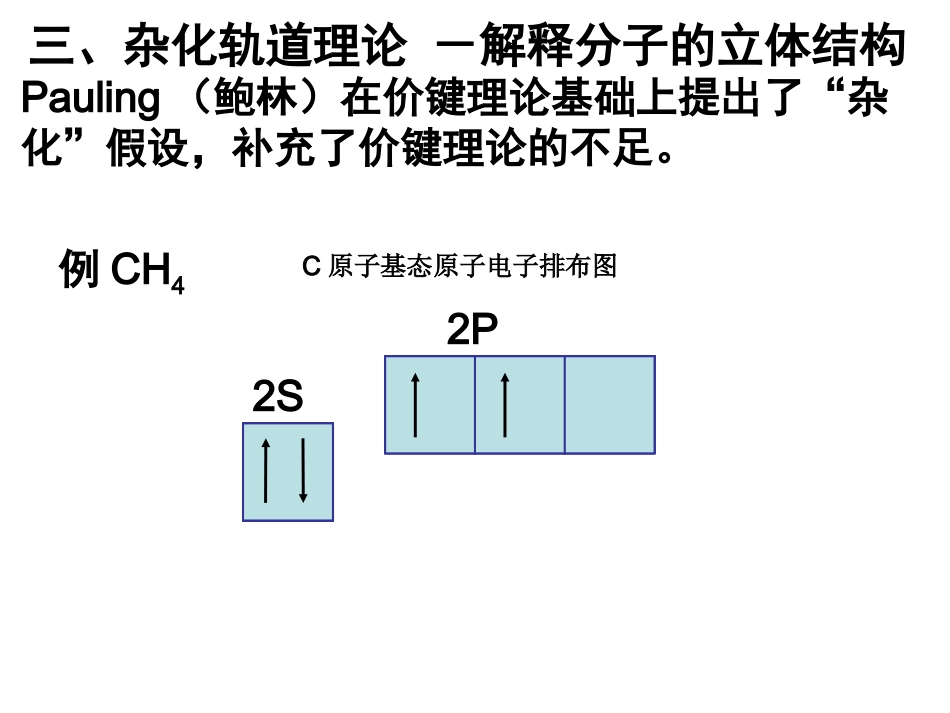
2P三、杂化轨道理论-解释分子的立体结构Pauling(鲍林)在价键理论基础上提出了“杂化”假设,补充了价键理论的不足
C原子基态原子电子排布图例CH42S2P三、杂化轨道理论-解释分子的立体结构(一)杂化理论要点:1
在形成分子时,每一原子中能量相近能量相近的“轨道”会发生重组,形成新的原子轨道,这个过程称“杂化”,新的原子轨道称“杂化轨道”
杂化前后原子“轨道”总数不变,但能量趋于平均化,“杂化轨道”对称性更高,利于成键
原子可用“杂化轨道”与其它原子的轨道重叠形成共价键
Pauling(鲍林)在价键理论基础上提出了“杂化”假设,补充了价键理论的不足
(二)杂化类型(二)杂化类型1、sp3杂化:例CH4sp3杂化轨道的形成过程xyzxyzzxyzxyz109°28′基态原子激发态原子1个S轨道和3个P轨道4个相同的SP3杂化轨道混杂实例分析2:试分析BeCl2分子的形成和空间构型
2个含有单电子的2s轨道和2px轨道进行sp杂化,组成夹角为1800的2个能量相同的sp杂化轨道,所以BeCl2分子的空间构型为直线型
sp杂化轨道的形成过程xyzxyzzxyzxyz180°实例分析2:试说明BF3分子的空间构型
1个2s轨道和2个2p轨道进行sp2杂化,形成夹角均为1200的3个完全等同的SP2杂化轨道
所以BF3分子的空间构型为平面正三角型
sp2杂化轨道的形成过程xyzxyzzxyzxyz120°杂化类型spsp2sp3参与杂化的原子轨道1个s+1个p1个s+2个p1个s+3个p杂化轨道数2个sp杂化轨道3个sp2杂化轨道4个sp3杂化轨道杂化轨道间夹角18001200109