第三单元《物质构成的奥秘》复习学案班级姓名【考纲要求】⒈了解原子、分子、离子的概念,⒉了解原子、分子、离子是怎样构成物质的⒊知道原子的构成,能看懂简单的原子结构示意图⒋知道元素及其分类、能正确书写常见元素的名称和符号⒌知道相对原子质量【复习内容】教材第三单元【要点梳理】知识点1分子与原子分子、原子比较分子原子定义分子是保持物质最小的微粒原子是中的最小微粒
性质体积和质量都、都在不断;之间都有联系分子是由构成的
分子、原子都是构成物质的微粒
区别化学变化中,分子,原子
〖化学反应的实质〗在化学反应中分子分裂为,原子重新组合成新的
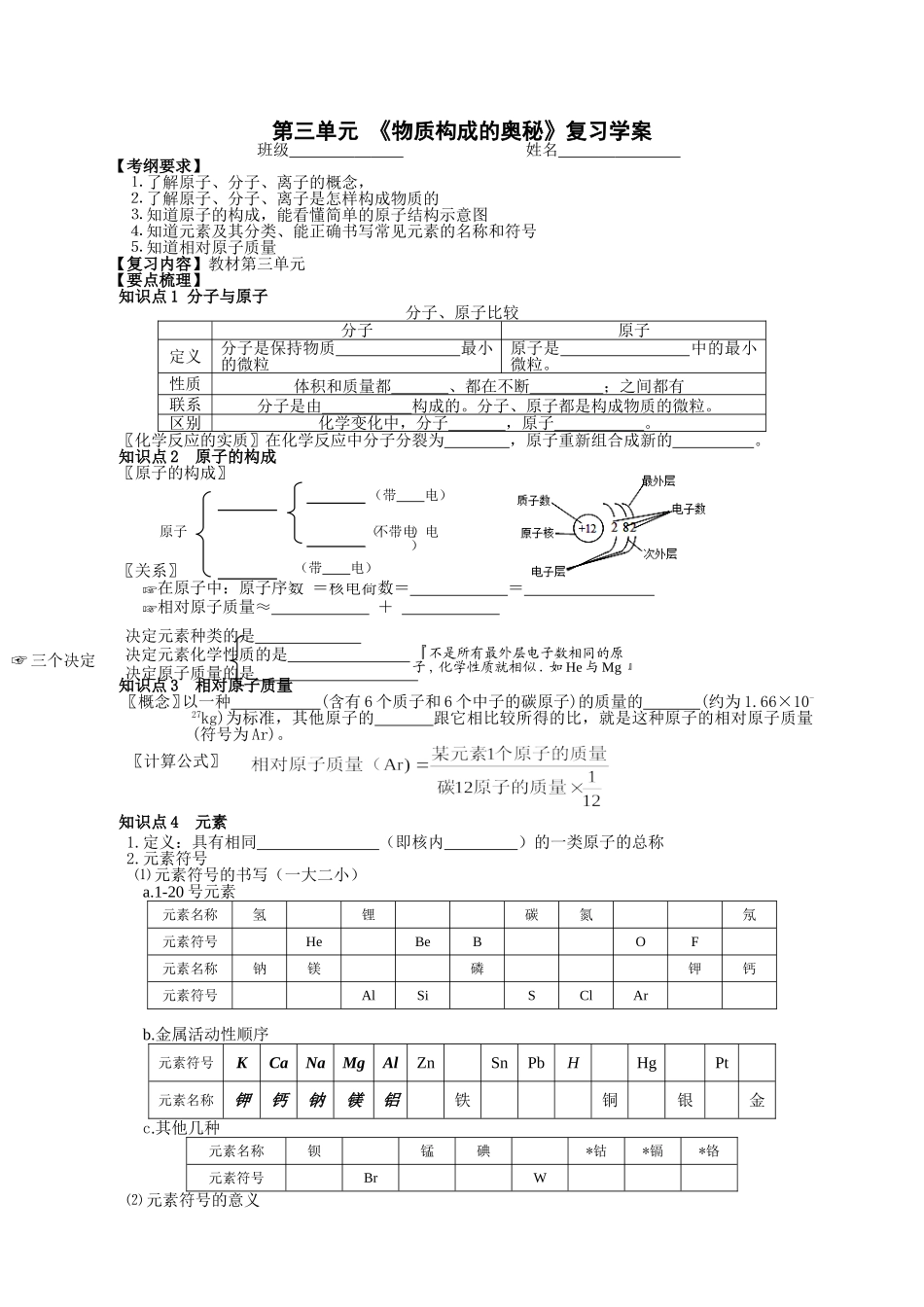
知识点2原子的构成〖原子的构成〗〖关系〗☞在原子中:原子序数=核电荷数==☞相对原子质量≈+知识点3相对原子质量〖概念〗以一种(含有6个质子和6个中子的碳原子)的质量的(约为1
66×10-27kg)为标准,其他原子的跟它相比较所得的比,就是这种原子的相对原子质量(符号为Ar)
知识点4元素1
定义:具有相同(即核内)的一类原子的总称2
元素符号⑴元素符号的书写(一大二小)a
1-20号元素元素名称氢锂碳氮氖元素符号HeBeBOF元素名称钠镁磷钾钙元素符号AlSiSClArb
金属活动性顺序元素符号KCaNaMgAlZnSnPbHHgPt元素名称钾钙钠镁铝铁铜银金c
其他几种元素名称钡锰碘*钴*镉*铬元素符号BrW⑵元素符号的意义(带电)(不带电)电)(带电)原子决定元素种类的是决定元素化学性质的是决定原子质量的是☞三个决定『不是所有最外层电子数相同的原子,化学性质就相似
如He与Mg』〖计算公式〗意义实例(以N为例)表示某种元素表示该元素的一个原子[温馨提示]☞①有些元素符号还可表示一种单质如Fe、He、C、Si☞②当元素符号前的化学计量数为不是“1”的其他数字时,只有,没有,如3H:表示⑶元素周期表---发现:门捷列夫⒊离子1概念:带电的或叫离子