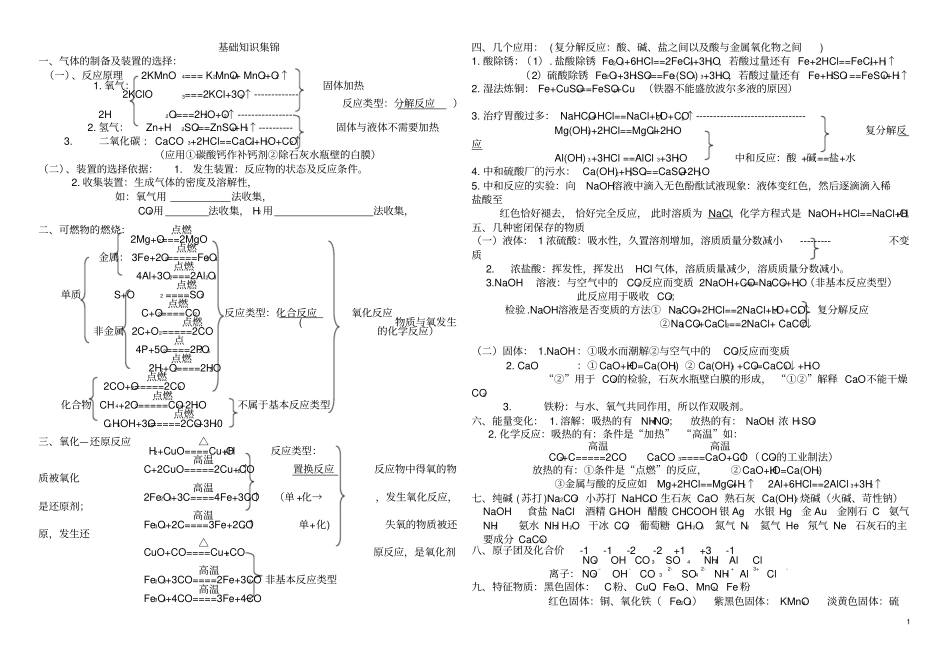
1基础知识集锦一、气体的制备及装置的选择:(一)、反应原理2KMnO4===K2MnO4+MnO2+O2↑1
氧气:固体加热2KClO3===2KCl+3O2↑-------------反应类型:分解反应)2H2O2===2H2O+O2↑-----------------2
氢气:Zn+H2SO4==ZnSO4+H2↑----------固体与液体不需要加热3
二氧化碳:CaCO3+2HCl==CaCl2+H2O+CO2↑(应用①碳酸钙作补钙剂②除石灰水瓶壁的白膜)(二)、装置的选择依据:1
发生装置:反应物的状态及反应条件
收集装置:生成气体的密度及溶解性,如:氧气用法收集,CO2用法收集,H2用法收集,二、可燃物的燃烧:点燃2Mg+O2===2MgO点燃金属:3Fe+2O2=====Fe3O4点燃4Al+3O2===2Al2O3点燃单质S+O2====SO2点燃C+O2====CO2反应类型:化合反应氧化反应点燃(物质与氧发生非金属2C+O2=====2CO的化学反应)点4P+5O2====2P2O5点燃2H2+O2====2H2O点燃2CO+O2=====2CO2点燃化合物CH4+2O2=====CO2+2H2O不属于基本反应类型点燃C2H5OH+3O2=====2CO2+3H20三、氧化—还原反应△H2+CuO====Cu+H2O反应类型:高温C+2CuO=====2Cu+CO2↑置换反应反应物中得氧的物质被氧化高温2Fe2O3+3C====4Fe+3CO2↑(单+化→,发生氧化反应,是还原剂;高温Fe3O4+2C====3Fe+2CO2↑单+化)失氧的物质被还原,发生还△CuO+CO====Cu+CO2原反应,是氧化剂高温Fe2O3+3CO====2Fe+3CO2非基本反应类型高温Fe3O4+4CO====3Fe+4CO2四、几个应用:(复分解反应:酸、碱、盐