第5讲化学反应与能量[最新考纲]1.能说明化学反应中能量转化的主要原因,知道化学变化中常见的能量转化形式
了解化学能与热能的相互转化及其应用
了解吸热反应、放热反应、反应热(焓变)等概念
能正确书写热化学方程式,能用盖斯定律进行有关反应热的简单计算
常考点一正确理解反应热准确判断吸热与放热[知识特训]1.通过判断理解反应热的相关概念(1)所有的燃烧反应都是放热反应,所以不需要加热就能进行(×)(2)反应物的总能量低于生成物的总能量时,一定不能发生反应(×)(3)物理变化过程中,也可能有热量的变化(√)(4)C(石墨,s)===C(金刚石,s)ΔH>0,说明石墨比金刚石稳定(√)(5)一个反应的焓变因反应物的用量和反应条件的改变而发生改变(×)(6)催化剂能改变反应的焓变(×)(7)已知S(l)+O2(g)===SO2(g)ΔH=-293
23kJ·mol-1,则S(s)+O2(g)===SO2(g)反应放出的热量大于293
23kJ·mol-1(×)(8)同温同压下,H2(g)+Cl2(g)===2HCl(g),在光照和点燃条件下的ΔH不同(×)2.化学键与反应过程的关系下表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ):物质H2(g)O2(g)H2O(g)能量436496926(1)反应2H2(g)+O2(g)===2H2O(g)是放热(填“吸热”或“放热”)反应,这说明2molH2(g)和1molO2(g)具有的能量比2molH2O(g)具有的能量高(填“高”或“低”)
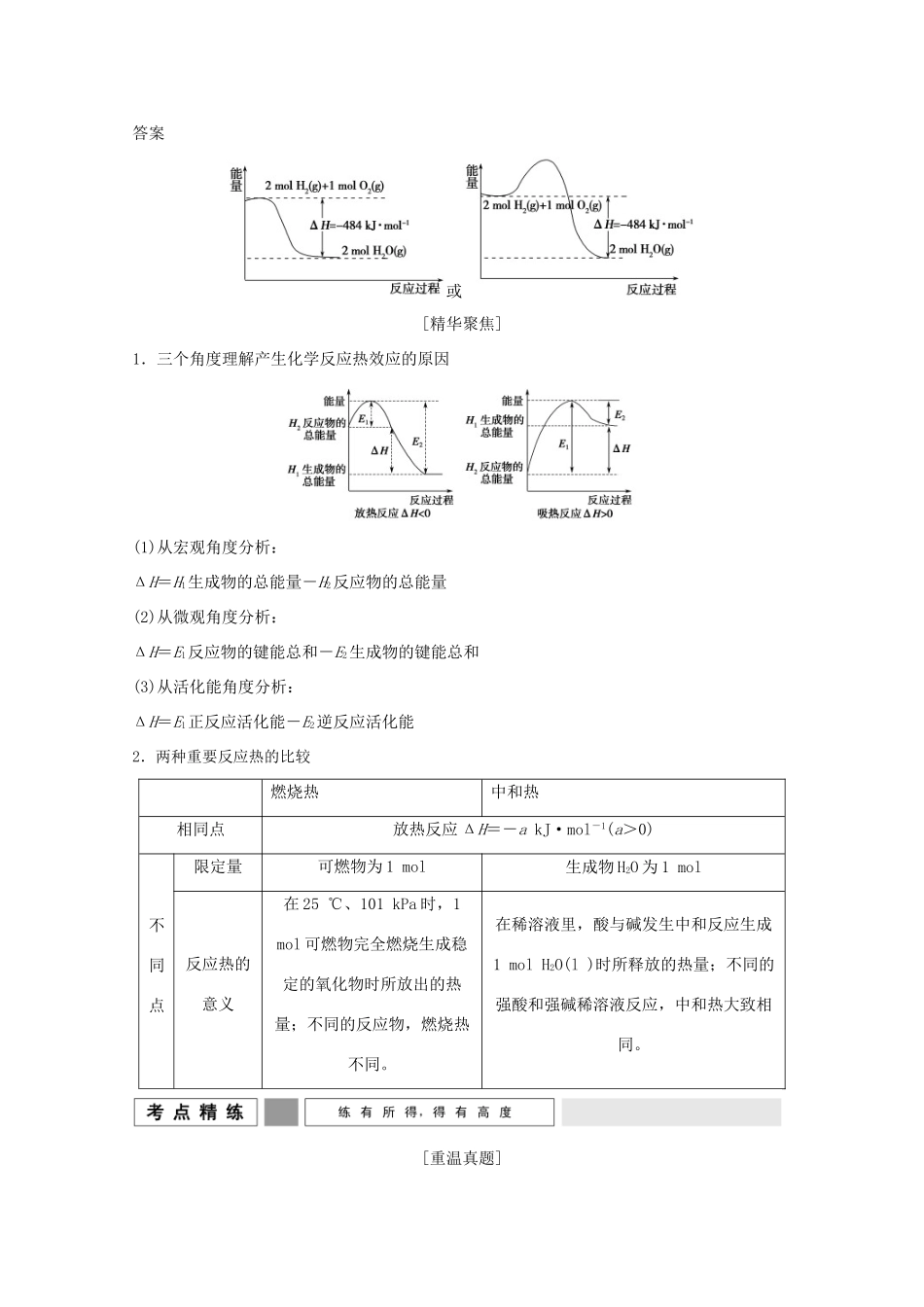
(2)请用图示表示出2molH2(g)与1molO2(g)生成2molH2O(g)的反应过程:答案或[精华聚焦]1.三个角度理解产生化学反应热效应的原因(1)从宏观角度分析:ΔH=H1生成物的总能量-H2反应物的总能量(2)从微观角度分析:ΔH=E1反应物的键能总和-E2生成物的键能总