专题讲座四加试第30题——基本概念、基本理论综合1.(2016·浙江4月选考,30)氨气及其相关产品是基本化工原料,在化工领域中具有重要的作用
(1)以铁为催化剂,0
6mol氮气和1
8mol氢气在恒温、容积恒定为1L的密闭容器中反应生成氨气,20min后达到平衡,氮气的物质的量为0
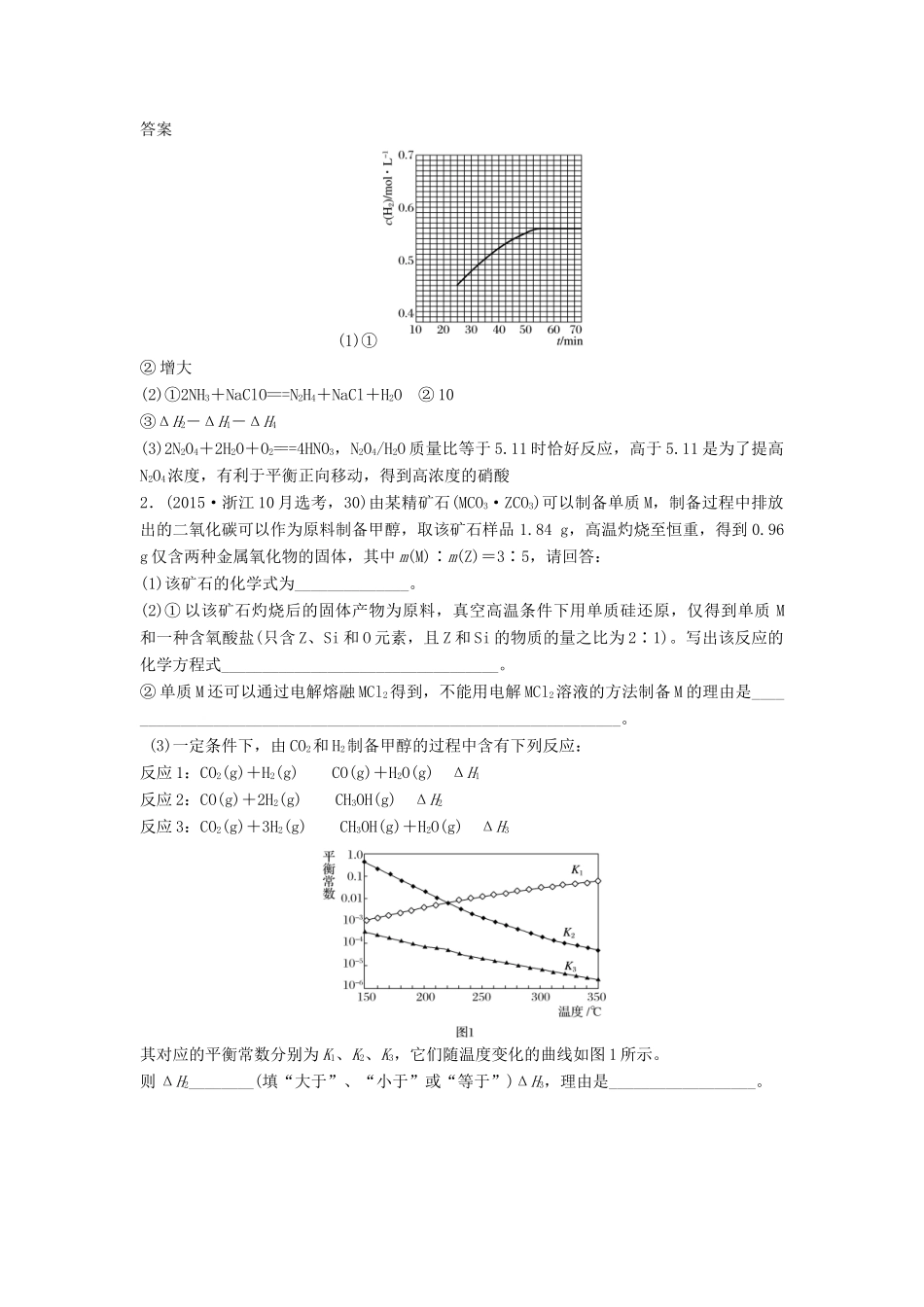
①在第25min时,保持温度不变,将容器体积迅速增大至2L并保持恒容,体系达到平衡时N2的总转化率为38
2%,请画出从第25min起H2的物质的量浓度随时间变化的曲线
②该反应体系未达到平衡时,催化剂对逆反应速率的影响是______(填“增大”、“减少”或“不变”)
(2)①N2H4是一种高能燃料,有强还原性,可通过NH3和NaClO反应制得,写出该制备反应的化学方程式_________________________________________________________________________________________________________________________________
②N2H4的水溶液呈弱碱性,室温下其电离常数K1=1
0×10-6,则0
01mol·L-1N2H4水溶液的pH等于________(忽略N2H4的二级电离和H2O的电离)
③已知298K和101kPa条件下:N2(g)+3H2(g)===2NH3(g)ΔH12H2(g)+O2(g)===2H2O(l)ΔH22H2(g)+O2(g)===2H2O(g)ΔH34NH3(g)+O2(g)===2N2H4(l)+2H2O(l)ΔH4则N2H4(l)的标准燃烧热ΔH=_____________________________________________
(3)科学家改进了NO2转化为HNO3的工艺(如虚框所示),在较高的操作压力下,提高N2O4/H2O的质量比和O