高中化学学习材料(灿若寒星**整理制作)课时作业16离子晶体时间:45分钟满分:100分一、选择题(共48分)1.下列各组中的两种固态物质熔化或升华时,克服的微粒间相互作用力属于同种类型的是()A.碘和氯化钾B.金刚石和重晶石C.二氧化硅和干冰D.软脂酸甘油酯和冰醋酸解析:A项碘克服分子间作用力,氯化钾克服离子键;B项金刚石克服共价键,重晶石克服的是离子键;C项二氧化硅克服共价键,干冰克服分子间作用力;D项均克服分子间作用力
答案:D2.金属晶体和离子晶体是重要晶体类型
下列关于它们的说法中正确的是()A.金属晶体和离子晶体都能导电B.在镁晶体中,1个Mg2+只与2个价电子存在强烈的相互作用C.金属晶体和离子晶体都可采取“紧密堆积”方式,原子晶体都可采取“非紧密堆积”方式D.金属晶体和离子晶体中分别存在金属键和离子键等相互作用,很难断裂,因而都具有延展性解析:离子晶体中的离子不是自由移动的离子,不能导电,A项不正确;镁晶体中的自由电子被整个晶体所共有,不属于某个Mg2+,B项不正确;离子晶体不具有延展性,D项错误
答案:C3.根据题表给出的几种物质的熔、沸点数据,判断下列有关说法错误的是()晶体NaClMgCl2AlCl3SiCl4单质B熔点/℃801714180-702300沸点/℃14651412160582500A
SiCl4是分子晶体B.单质B可能是原子晶体C.AlCl3加热能升华D.NaCl的键的强度比MgCl2的小解析:由表中所给数据,知SiCl4熔、沸点低,应为分子晶体,A正确
单质B熔、沸点很高,可能是原子晶体,B正确
AlCl3的沸点低于熔点,可以升华,C正确
本题数据表明,NaCl的熔、沸点高于MgCl2的,故不能说明NaCl键的强度比MgCl2小,D错
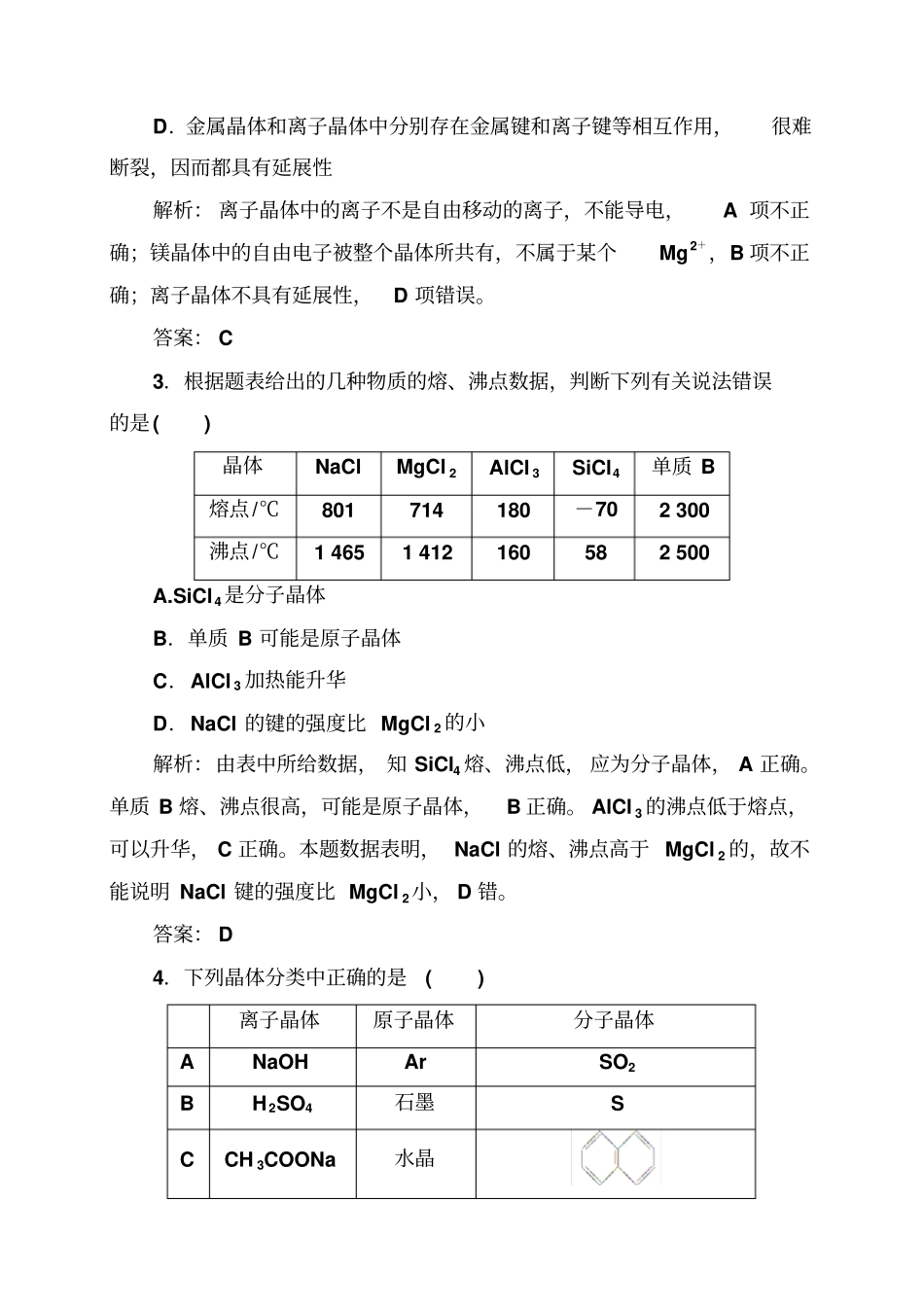
答案:D4.下列晶体分类中正确的是()离子晶体原子晶体分子晶体ANaOHArSO2BH2SO4石墨S