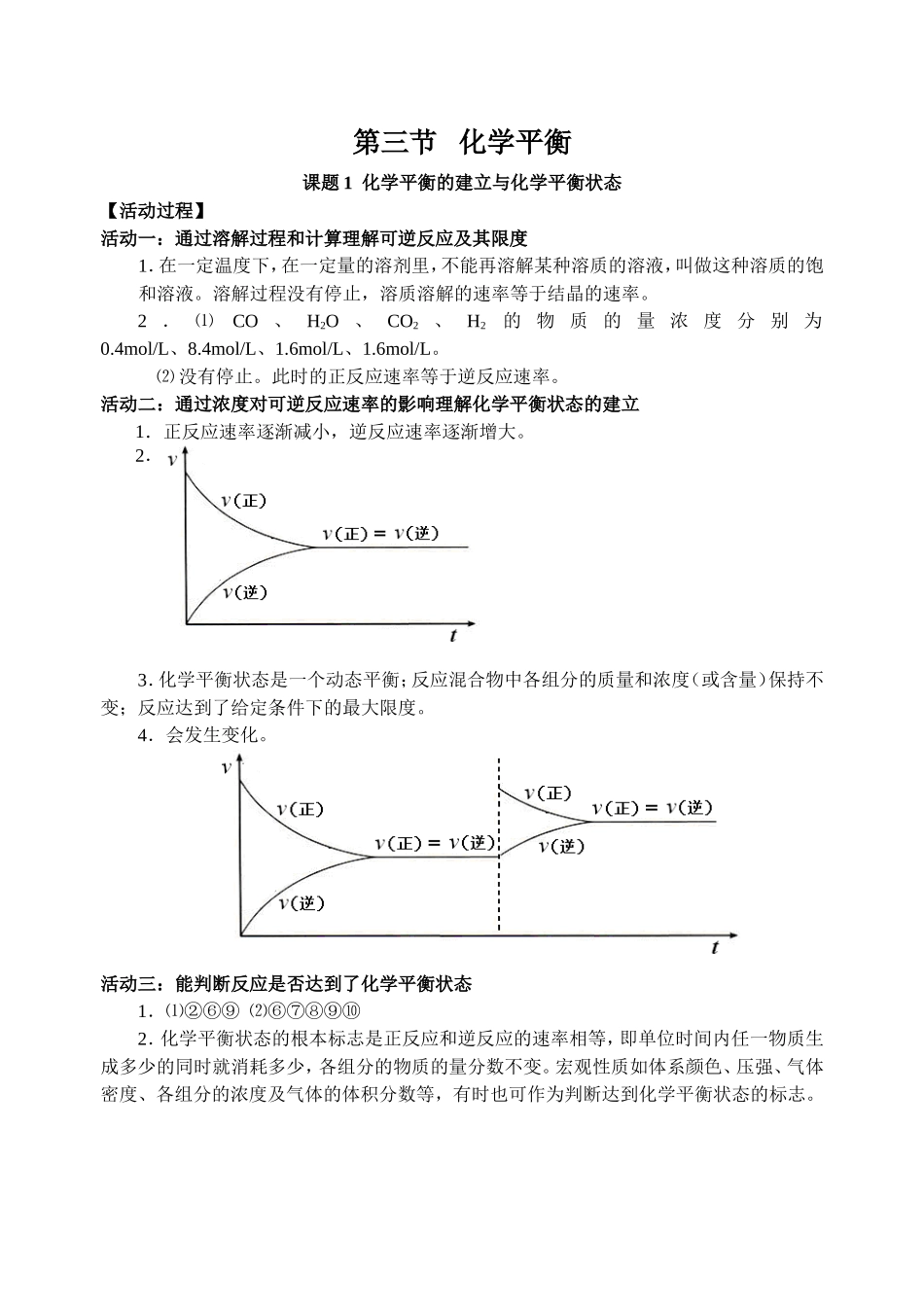
第三节化学平衡课题1化学平衡的建立与化学平衡状态【学习目标】1.进一步认识可逆反应及其限度
2.能描述化学平衡建立的过程
【活动过程】活动一:通过溶解过程和计算理解可逆反应及其限度1.什么是饱和溶液
饱和溶液中溶质的溶解过程完全停止了吗
为什么溶液中溶质的质量不变
2.在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,叫做可逆反应
可逆反应不能进行到底
在1L的密闭容器中,将2
0molCO和10molH2O混合加热到800℃,发生反应CO+H2OCO2+H2,当反应体系中各物质的浓度不再改变时,CO转化为CO2的转化率为80%
⑴求此时密闭容器中各物质的物质的量浓度
⑵你认为此时化学反应停止了吗
为什么体系中各物质的浓度会不发生变化
活动二:通过浓度对可逆反应速率的影响理解化学平衡状态的建立1.对于一般的可逆反应,你认为从开始到反应体系中各物质的浓度不再改变,正、逆反应速率的变化趋势是什么
2.画出正、逆反应速率随时间变化的曲线图
3.上述“正反应速率等于逆反应速率”的状态就是化学平衡状态
请你进一步描述化学平衡状态还有哪些特征
4.当一个可逆反应已经达到平衡状态后,假如此时增加反应物浓度,你认为平衡状态是否会发生变化
进一步画出增加反应物浓度后,正、逆反应速率随时间变化的曲线图
活动三:能判断反应是否达到了化学平衡状态1.通过具体实例,判断反应是否达到了化学平衡状态
⑴对于可逆反应“2HI(g)H2(g)+I2(g)”,下列哪些描述可以作为已达平衡状态的标志
①单位时间内生成nmolH2的同时生成nmolHI②一个H-H键断裂的同时有两个H-I键断裂③百分组成w(HI)=w(I2)④反应速率v(H2)=v(I2)=v(HI)/2时⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1时⑥温度和体积一定时,某一生成物浓度不再变化⑦温度和体积一定时,容器内压强不