第十单元实验活动6酸、碱的化学性质基础知识梳理部分一、常见的酸:注意:酸的化学性质盐酸硫酸1、组成(元素)2、构成(电离出的离子)3、物质类别酸酸4、物理性质无色液体,具有性,浓盐酸能冒,具有气味
无色粘稠液体,浓硫酸具有和的物理特性
5、化学性质1
酸使紫色石蕊试液变__使无色酚酞试液______盐酸使紫色石蕊试液_____,使无色酚酞试液______硫酸使紫色石蕊试液_______,使无色酚酞试液_______2
酸+_____→盐+氢气Zn+HCl-Zn+H2SO4-3
酸+金属氧化物→+水Fe2O3+HCl-ZnO+H2SO4-4
酸+_______→盐+水NaOH+HCl-Zn(OH)2+H2SO4-6、用途①②③化工原料①②③化工原料④精炼石油7、其它1、浓硫酸的特性_____________、____________、______________、_______________2、浓硫酸的稀释操作___________________________________________事故处理:①浓硫酸沾到皮肤或衣物上应:
②氢氧化钠溶液沾到皮肤或衣物上应:
3、遇水放热的物质有、、
具有吸水性的物质有______、________、____________,可做_______剂4、干燥剂的选择技巧选择干燥剂的原则是:干燥剂不能与被干燥的气体反应
可干燥气体(可以的请划线,不可以的划掉)不可干燥的气体浓硫酸CO2、SO2、HCl、O2、H2、CO、NH3、N2_______CaONaOHNH3、O2、H2、CO、CO2、N2______、______、_____5、浓硫酸和氢氧化钠具有气气强烈的腐蚀性,因此二者不可做食品干燥剂
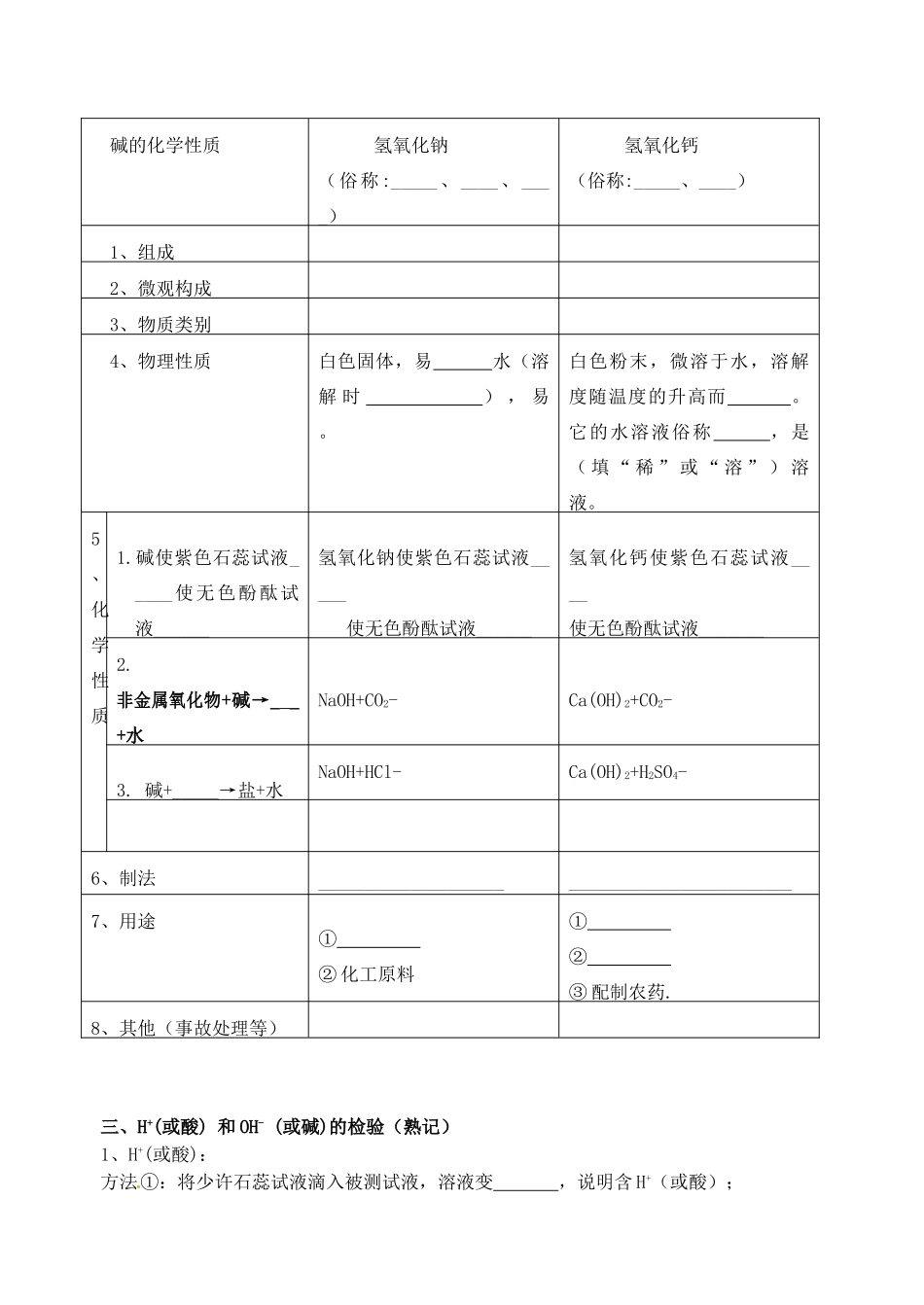
二、常见的碱的化学性质:三、H+(或酸)和OH-(或碱)的检验(熟记)1、H+(或酸):方法①:将少许石蕊试液滴入被测试液,溶液变,说明含