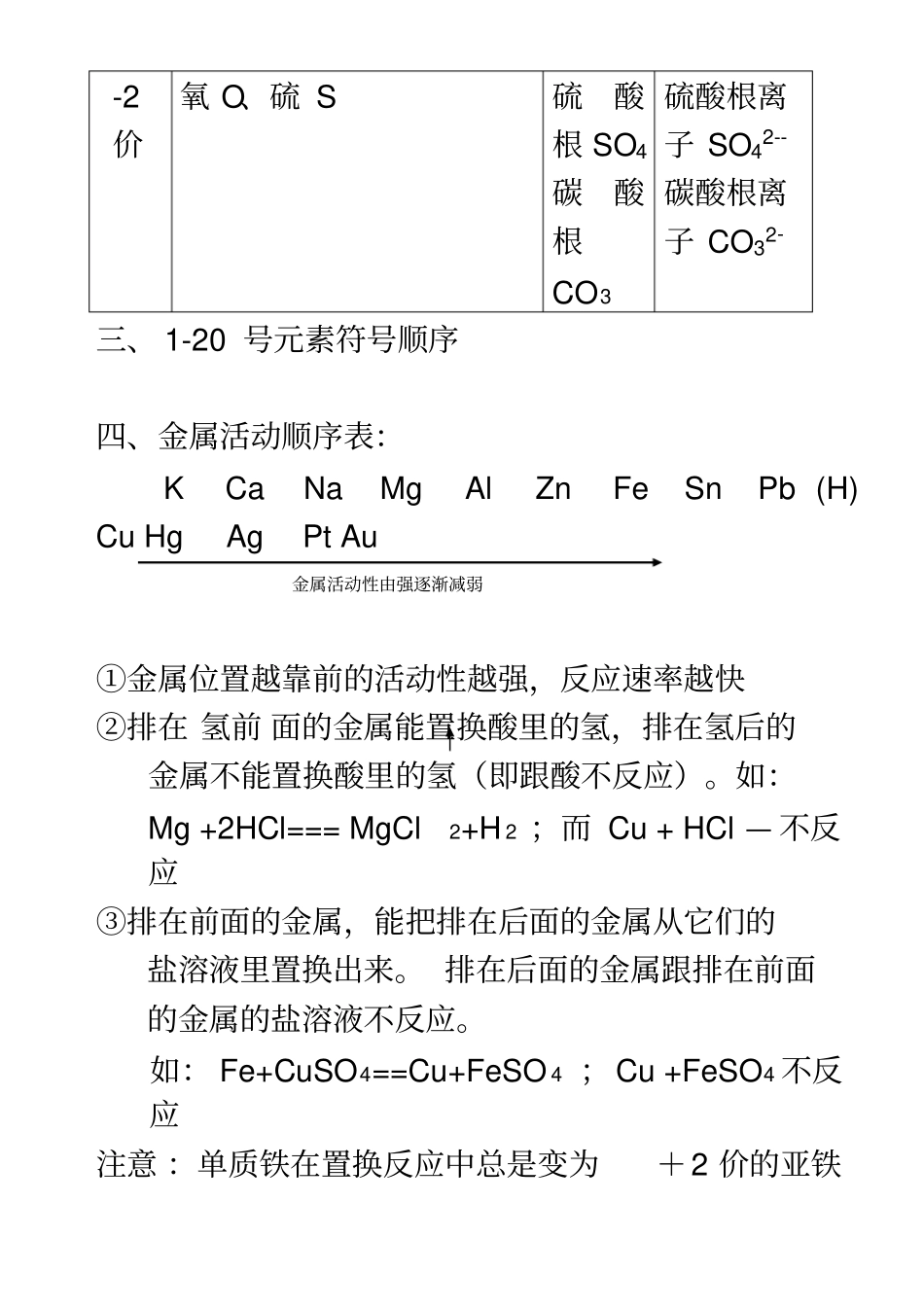
化学升中必考识记(把记忆落到实处是学好化学的有效方法)班别: _______ 姓名: _________ 一、元素符号氢 H 氦 He 碳 C 氧 O 氟 F 氖 Ne 钠 Na 镁Mg 铝 Al 硅 Si 磷 P 硫 S 氯 Cl 氩 Ar 钾 K 钙 Ca 铁 Fe 锌 Zn 铜 Cu 钡 Ba 银 Ag 汞 Hg 锰Mn 金 Au 碘 I 铂 Pt 二、原子团及元素化合价化合价元素原子团+1价氢 H、钠 Na、钾 K、银Ag 铵根NH 4铵根离子NH 4++2价镁 Mg、钙 Ca、铜 Cu、锌Zn、钡 Ba、亚铁 Fe +3价铝 Al 、铁 Fe -1价氯 Cl氢氧根 OH 硝酸根NO 3氢氧根离子 OH--硝酸根离子 NO3---2价氧 O、硫 S 硫酸根 SO4碳酸根CO3硫酸根离子 SO42--碳酸根离子 CO32-三、 1-20 号元素符号顺序四、金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au ①金属位置越靠前的活动性越强,反应速率越快②排在 氢前 面的金属能置换酸里的氢,排在氢后的金属不能置换酸里的氢(即跟酸不反应)
如:Mg +2HCl=== MgCl2+H 2 ;而 Cu + HCl — 不反应③排在前面的金属,能把排在后面的金属从它们的盐溶液里置换出来
排在后面的金属跟排在前面的金属的盐溶液不反应
如: Fe+CuSO4==Cu+FeSO 4 ; Cu +FeSO4 不反应注意 :单质铁在置换反应中总是变为+2 价的亚铁金属活动性由强逐渐减弱五、溶解性规律“钾钠铵硝全溶、氯全溶除银盐,硫酸钡不银钙微、氢氧钾钠铵钡溶”(1)酸:所有酸全部溶于水(2)碱: KOH 、NaOH、NH 4OH、Ba(OH) 2溶于水, Ca(OH)2微溶,其余不溶硝酸盐:全溶(3)盐: 碳酸盐: K 2CO3、Na2