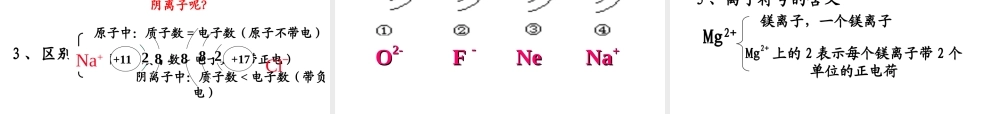课题 课题 22 原子的构成原子的构成 (二) 1 、什么是原子
2 、原子是怎样构成的
3 、为什么整个原子不显电性
温故知新原子是化学变化中的最小粒子
原子是化学变化中的最小粒子
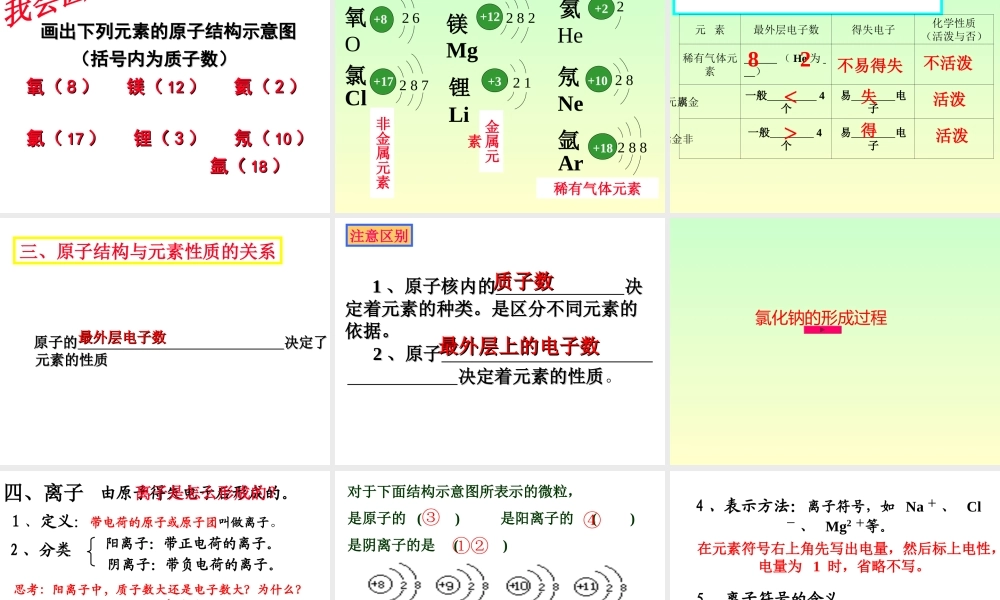
原子核所带的正电荷总数与核外电子所带的负电荷总数相等,所以整个原子不显电性
原子原子核( + )核外电子(一)质子( + )中子(不带电)核电荷数 = 核内质子数 = 核外电子数 若将原子比做一个庞大的体育场,而原子核只相当于一只小蚂蚁
电子运动没有固定的轨道,但电子运动没有固定的轨道,但有经常出现的区域,科学家把这样的区有经常出现的区域,科学家把这样的区域称为域称为电子层
核外电子的分层运动又称为核外电子的分层排布,那么核外电子是如何分层排布的呢
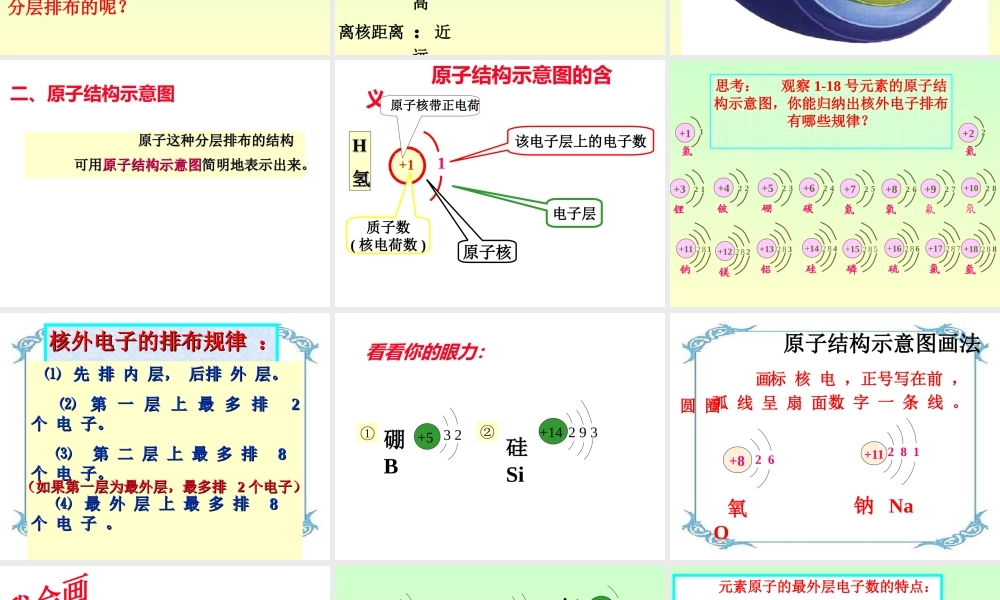
123 一、核外电子的分层排布 电 子 层 数 : 一 二 三 四 五 六 七 … 符号 : K L M N O P Q电子能量 :低 高离核距离 :近 远 原子这种分层排布的结构 原子这种分层排布的结构 可用可用原子结构示意图原子结构示意图简明地表示出来
简明地表示出来
二、原子结构示意图 原子结构示意图的含义HH氢氢+11电子层该电子层上的电子数原子核质子数( 核电荷数 ) 原子核带正电荷+11氢+22氦+32锂1+42铍2+52硼3+62碳4+72氮5+82氧6 +92氟7+102氖8+11 2钠8 1 +12 2镁8 2+13 2铝8 3+14 2硅8 4+15 2磷8 5+16 2硫8 6+17 2氯8 7 +18 2氩8 8思考: 观察 1-18 号元素的原子结构示意图,你能归纳出核外电子排布有哪些规律
核外电子的排布规律 :核外电子的排布规律 : ⑴ ⑴ 先 排 内 层, 后排 外 层
先 排 内 层, 后排 外 层
⑵ ⑵ 第 一 层 上 最 多 排 第 一 层 上 最 多 排 2 2 个 电 子