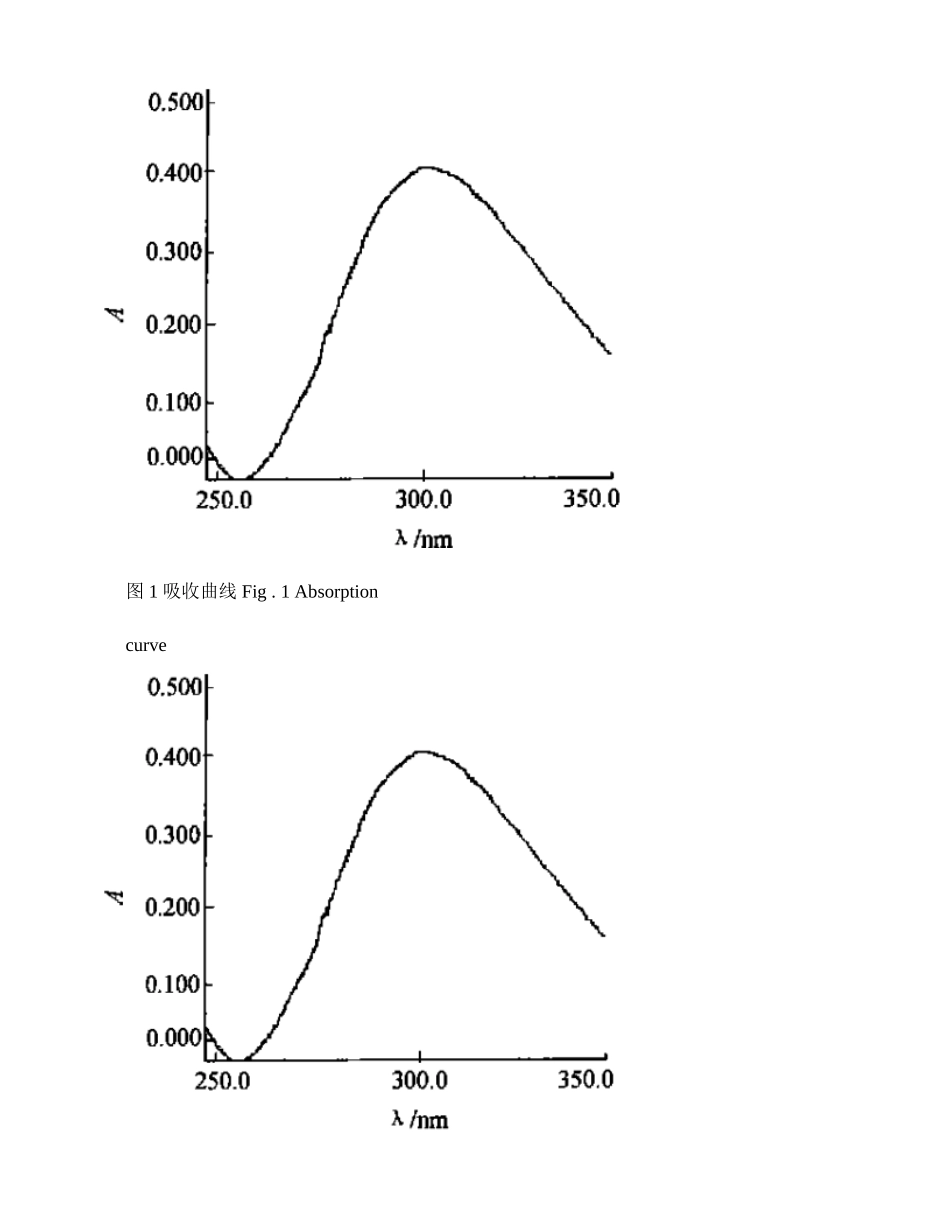
分光光度法测定多巴胺王怀友X,孙悦,唐波(山东师范大学化学系,济南250014摘要:根据多巴胺与亚硝酸钠在pH5
90时的反应产物在300nm处有最大吸收,建立了测定多巴胺注射液中多巴胺浓度的分光光度法
多巴胺质量浓度在0~10LgPmL范围内与吸光度之间遵从朗伯比尔定律,表观摩尔吸光系数为1
85@104L#mol-1#cm-1,检测限为0
1LgPmL
试验了pH、放置时间、加热时间、干扰离子等对测定的影响
本法可用于注射液中多巴胺含量的测定,与药典规定方法对照,结果吻合
关键词:分光光度法;多巴胺;亚硝酸钠;多巴胺注射液中图分类号:O657132文献标识码:A文章编号:1000-0720(200301-0045-03多巴胺是一种神经传递物质,在体内是合成去甲肾上腺素的直接前体,具有重要的生理作用
作为药物,能增强心肌收缩力,对内脏血管有扩张作用,增加血流量,有利于改善休克时重要脏器的血液供应,适用于感染性、心源性、失血性休克以及心脏停搏时起搏升压
显然,建立灵敏简便的测定方法,具有十分重要的意义
现已报道的测定方法有荧光光度法[1],色谱分析法[2]和电化学分析方法[3]
龙云等[4]研究了多巴胺与四氯苯醌之间的荷移反应,用分光光度法测定针剂中的多巴胺,E值仅为1
63@103;文献[5]从甜马铃薯中提取多酚氧化酶,将多巴胺氧化为相应多巴胺色素,建立了测定药剂中多巴胺的分光光度法,但操作繁杂
本研究依据多巴胺与亚硝酸钠在水介质中即可生成有较高吸光度产物的反应,建立了测定多巴胺注射液中多巴胺含量的分光光度法
该法操作简便,灵敏迅速,有宽的线性范围,与英国药典规定的高效液相色谱法[6]对照,结果吻合
1实验部分1
1仪器UV-265紫外可见分光光度计(日本岛津;pHS-3C型酸度计(上海雷磁仪器厂
多巴胺标准储备液100LgPmL(化学对照品,中国药品生物制品检定所,准确